Afamin/Wnt3a複合体の姿と動きの観察に成功 ―疎水性ポケットの重要性を明らかに―
金沢大学大学院新学術創成研究科ナノ生命科学専攻博士後期課程の市田光、水野皓介(現・大阪大学蛋白質研究所 博士研究員)、ナノ生命科学研究所(WPI-NanoLSI)の古寺哲幸教授、ホルガー・フレクシグ特任准教授、大阪大学蛋白質研究所の戸田聡准教授の共同研究グループは、血清タンパク質であるAfaminが、脂質修飾シグナル分子のWnt3aを安定化して運ぶ際の姿と動きの観察に成功しました。さらに、この二つの分子が正しく結合するためには、Afaminが持つ、Wnt3aの脂質を収容するための疎水性のポケットが必須であることを明らかにしました。
Wntタンパク質は、体や臓器の形づくりから、それらを健康に保つための過程で欠かせない大切な分子です。しかし、水に溶けにくい性質(疎水性)を持つため、生体内では他の分子と協力しながら、水に溶けやすくなることで、安定して目的の細胞に運搬されます。本研究では、Wnt3aが別のタンパク質に助けられながら安定して運ばれる仕組みの一端が示されました。
本研究で得られた知見は、Wnt3aが関わる生命現象の仕組みの理解を深めるとともに、将来的には生体外での組織構築技術や再生医療分野への展開が期待されます。
本研究成果は、2026年4月15日(現地時間)に米国化学会機関誌『Nano Letters』のオンライン版に掲載されました。
【研究の背景】
Wntタンパク質は、形態形成や幹細胞維持などに重要な役割を果たす細胞間シグナル分子です。Wntタンパク質は脂質分子による修飾を受けることで疎水性が高まり、水中において単独では安定に存在しにくいことが知られています。そのため、生体内の液性環境において、Wntタンパク質がどのように安定化され、輸送されているのかについては十分に解明されておらず、重要な研究課題となっていました。
Afaminは血清中に存在する糖タンパク質で、脂溶性分子を運ぶキャリアタンパク質として知られています。これまでに、AfaminがWnt3aと複合体を形成し、その生理活性を保ったまま可溶化することが報告されていましたが、実際に両者がどのような立体配置を取り、どのように動いているのかは分かっていませんでした。特に、Afaminの中央部に存在する水に溶けにくい疎水性分子を受け止める場所(疎水性ポケット、※1)が、Wnt3aの安定化や輸送にどう関わるかは未解明でした。
【研究成果の概要】
研究グループはまず、高速原子間力顕微鏡(高速AFM、※2)を用いて、Afamin単独分子の挙動を観察しました。その結果、Afaminが大小2つの球状ドメインの間でヒンジのように開閉する動きを示すことを明らかにしました(図1)。
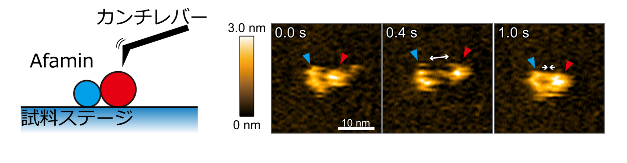
図 1:高速AFM観察の模式図(左)とAfaminの連続した高速AFM画像(右)。
Afaminは大きい部位(赤色)と小さい部位(水色)からなり、柔軟に伸縮する様子が観察された。
さらに、分子モデリングにより、この柔軟な運動がAfamin中央部の構造に由来することを示しました(図 2)。
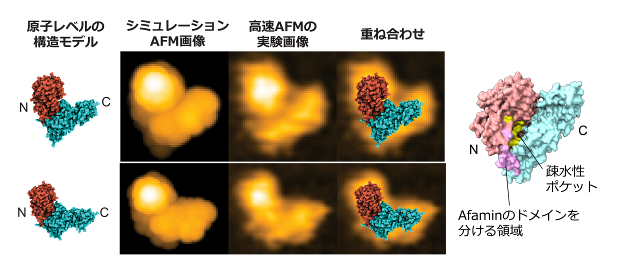
図 2:タンパク質の三次元原子構造モデルを推定する計算科学的手法による高速AFM画像の解析(左)とその解析結果よって色分けされたAfaminの構造(右)。
ピンクで示した領域は特定の構造を持たない領域でこの領域の中心でN末端側ドメインとC末端側ドメインを区別できることを明らかにした。また黄色で示した疎水性ポケットはAfaminのほぼ中央に位置している。
次に、AfaminとWnt3aの複合体(Afamin/Wnt3a)を高速AFMで観察したところ、これまで直接見ることが難しかったAfamin/Wnt3a複合体の1分子の姿を捉えることに世界で初めて成功しました。観察の結果、この複合体は単一の静的な構造ではなく、Wnt3aが中央付近に位置する対称型構造と、片側に偏って位置する非対称型構造の2種類の構造をとり、それらが相互に移り変わることを見出しました。また、Wnt3aが結合すると、Afamin分子のゆらぎは、Afamin単独のときよりも小さくなり、構造の柔軟性が抑えられることも分かりました(図 3)。
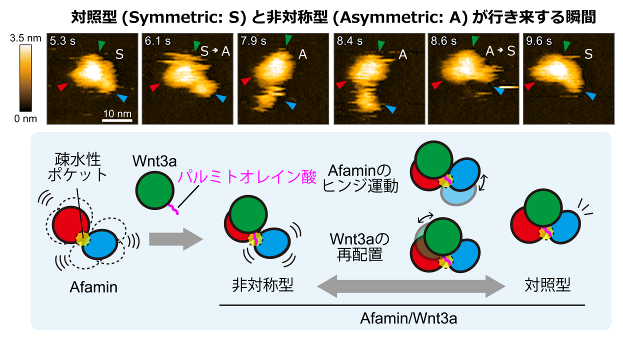
図 3:Afamin/Wnt3aの連続した高速AFM画像(上)とその運動のモデル(下)。
さらに、細胞膜上でAfaminとWnt3aの結合を観察したところ、Afaminの疎水性ポケットにわずかに変異を入れるだけでWnt3aとの結合が阻害されることが明らかになりました。この結果から、Wnt3aとの結合には、疎水性ポケットの全体構造が重要であることが示唆されました(図 4)。
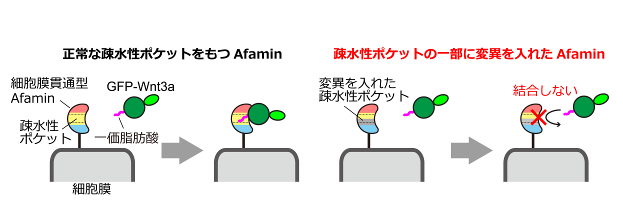
図 4:細胞表面に固定したAfamin変異体を用いた結合実験の概略図。
正常な疎水性ポケットをもつAfaminにはWnt3aが結合するが(左)、一部に変異が入るとWnt3aと結合しなくなる(右)。
本研究では、金沢大学ナノ生命科学研究所(WPI-NanoLSI)の特長の一つであるユニークな顕微鏡技術による分子動態の直接観察を中核として、溶液中で動くタンパク質複合体の形状変化を捉えました。加えて、その顕微鏡画像からタンパク質の三次元原子構造モデルを推定する計算科学的解析を組み合わせることで、観察像に対応する立体構造の理解を深めました。さらに、細胞工学的手法を用いた細胞環境下での結合評価法を組み合わせることで、脂質修飾タンパク質の輸送機構に新たな構造的知見を与えました。
【今後の展開】
本研究により、AfaminがWnt3aを単に保持するだけでなく、動的に構造を変化させながら輸送するキャリアとして機能している可能性が示されました。今後は、AfaminからWnt受容体や他の結合因子へWnt3aが受け渡される過程を直接観察することで、細胞外におけるWnt輸送機構の分子メカニズムの解明が期待されます。
用語解説
掲載論文情報
- 論文タイトル
- Structural Dynamics of the Afamin/Wnt3a Complex Mediated by the Afamin Hydrophobic Pocket (Afaminの疎水性ポケットを介したAfamin/Wnt3a複合体の構造動態)
- 著者
- Hikaru Ichida, Kosuke Mizuno, Romain Amyot, Kenichi Umeda, Satoshi Toda, Holger Flechsig, Noriyuki Kodera (市田光、水野皓介、Romain Amyot、梅田健一、戸田聡、Holger Flechsig、古寺哲幸)
- 掲載誌
- Nano Letters
- 掲載日
- 2026.05.15
- DOI
- 10.1021/acs.nanolett.5c05561
- URL
- https://doi.org/10.1021/acs.nanolett.5c05561

