タンパク質合成装置リボソームが持つ触手の はたらきの可視化に成功!
金沢大学ナノ生命科学研究所の今井大達日本学術振興会特別研究員,古寺哲幸教授,新潟大学理学部内海利男名誉教授の共同研究グループは,タンパク質合成装置リボソーム(※1)の構成成分の一つである触手タンパク質複合体「ストーク(※2)」の動きとはたらきの一端を可視化することに世界で初めて成功しました。
研究の背景
mRNAの遺伝情報に従いアミノ酸を連結させタンパク質を作る過程(翻訳)は,巨大分子集合体であるリボソームにさまざまなリボソーム結合タンパク質(翻訳因子)(※3)が作用して進行する生体内で最も複雑な反応系の一つです。新潟大学の内海名誉教授らはこれまで,タンパク質合成反応の進行に決定的な役割を果たすリボソーム構成成分として触手タンパク質複合体「ストーク」を見いだし,以前新潟大学大学院生であった今井氏らと共にその構造と機能について研究を進めてきました。これまでの研究結果から,古細菌の触手タンパク質aP1と触手タンパク質aP0はaP0•(aP1)2•(aP1)2•(aP1)2の七量体として存在し,各触手タンパク質はさまざまな翻訳因子と直接結合することでタンパク質合成を促進することが明らかとなっていました。一方で,リボソーム上の触手タンパク質複合体は,その柔軟性のためX線結晶構造解析やクライオ電子顕微鏡などの強力な構造生物学的手法を用いても解像されず,ストークの動的な作用実態は長らく解明されていませんでした。
研究成果の概要
本研究グループは,古細菌リボソームのストークの機能動態の解明に取り組みました。金沢大学が独自に開発してきた高速原子間力顕微鏡(高速AFM)(※4)を用いることで,これまで解像することが不可能だったリボソーム上の触手タンパク質複合体を初めて可視化し,ストークが少なくとも2状態のコンフォメーションをとることを見いだしました(図1)。さらに,ストークがペプチド伸長反応に重要な翻訳因子aEF2やaEF1Aをリボソームの周囲にかき集め,これらの局所濃度を上昇させた翻訳因子プールを形成することを明らかにしました(図2)。
このように,リボソームはストークの複数の天然変性領域という触手を伸ばし,その先端部分(C末端部分)を用いて翻訳因子をかき集めることでタンパク質合成反応を効率よく進めることが明らかとなりました。これらの成果は,さまざまな分子で混雑している細胞内において,リボソームが触手タンパク質複合体を介して効率的に翻訳因子を捕獲していることを示しており,タンパク質合成反応の根本原理の解明に貢献するものです。リボソームが触手タンパク質複合体を用いてタンパク質合成に必要な翻訳因子を集める様子は,鵜匠が多くの鵜を巧みにあやつり獲物である鮎をかき集める「鵜飼い」のようにみえます(図3)。
今後の展開
本研究は, リボソームのストークによって形成される翻訳因子プールの存在を立証し, 混雑した細胞内環境においてタンパク質合成という生命の根幹を担う現象が効率よく行われる分子機構の解明に向けた研究を大きく前進させました。この成果は,ヒト細胞内タンパク質はもちろんのこと,細胞に感染したウイルスのタンパク質が合成される仕組みについても新しい理解を提供するものです。今後はEF1AやEF2以外の翻訳に関わる他のさまざまな因子とリボソームの相互作用を高速AFMによって可視化することで,翻訳システム全般の仕組みの理解が深まることが期待されます。

図1. 高速AFMによって可視化された触手タンパク質複合体の動態
(A) 超好熱性古細菌Pyrococcus furiosus由来50Sリボソームの高速AFM像
(B) 触手タンパク質複合体の動態のモデル図
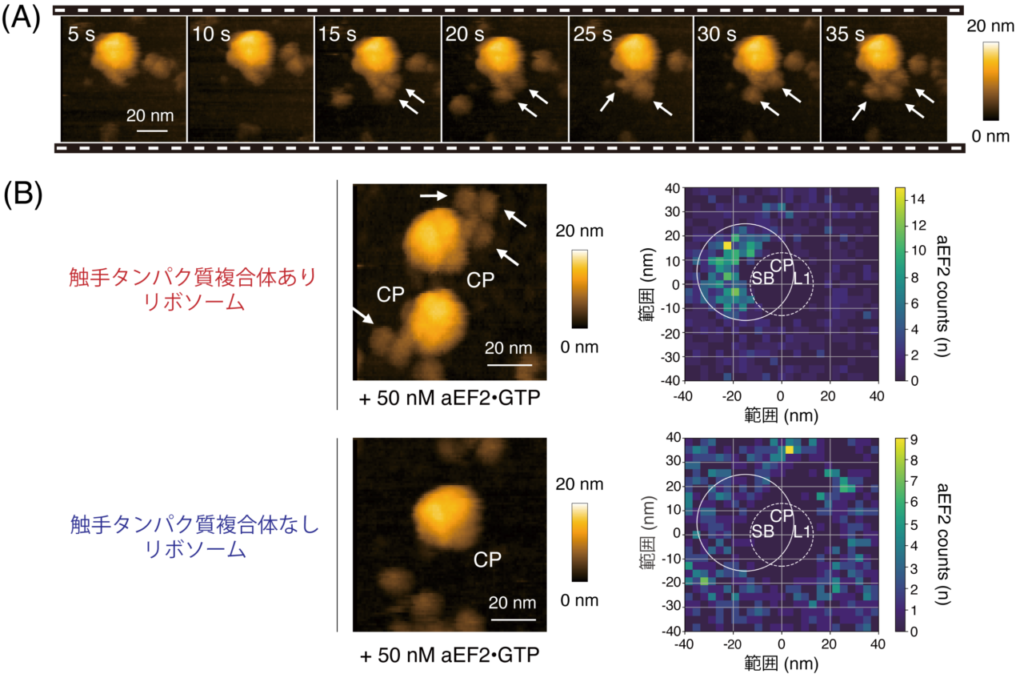
図2. 触手タンパク質複合体と翻訳因子の相互作用動態
(A) 翻訳伸長因子EF2が触手タンパク質複合体に集合していく様子
(B) 触手タンパク質複合体がリボソーム近傍の翻訳因子の局所濃度パターンに影響を及ぼす
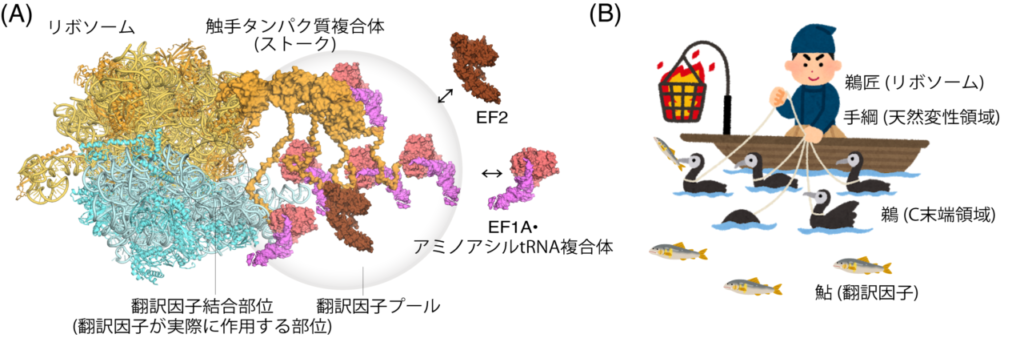
図3. 本研究のまとめ図
(A) リボソームは触手タンパク質複合体を介して翻訳因子の局所濃度を上昇させることで,効率よくかつ正確にタンパク質を合成する
(B) まるで「鵜飼い」のような触手タンパク質複合体のはたらき (イラストは、“いらすとや”からのものを一部改変して使用)
高速AFM動画に関するQRコード
図1(A)と図2(A)に関する高速AFMで撮影した動画は,以下のQRコードまたはURLで表示されるリンク先からご覧いただけます。


用語解説
掲載論文情報
- 論文タイトル
- Direct visualization of translational GTPase factor pool formed around the archaeal ribosomal P-stalk by high-speed AFM (古細菌リボソームPストーク周囲に形成されるGTPase翻訳因子プールの高速AFMによる可視化)
- 著者
- Hirotatsu Imai,Toshio Uchiumi,Noriyuki Kodera (今井大達, 内海利男, 古寺哲幸)
- 掲載誌
- Proceedings of the National Academy of Sciences of United States of America
- 掲載日
- 2020.12.07
- DOI
- 10.1073/pnas.2018975117
- URL
- https://www.pnas.org/content/early/2020/12/04/2018975117/tab-article-info
Funder
詳しくはこちら

