CRISPR-Cas9 がDNAを切断する瞬間の撮影に成功!
- 高速原子間力顕微鏡(高速AFM)を用いて、ゲノム編集ツールCRISPR-Cas9 によるDNA 切断を動画として撮影することに成功した。
- DNA 切断の際、Cas9 は大きな構造変化を起こすことが明らかになった。
- 本研究結果は、CRISPR-Cas9 を利用したゲノム編集技術の高度化の基盤となることが期待される。
概要
近年、生命の設計図であるゲノム情報(DNA の塩基配列)を書き換える「ゲノム編集」(注1)技術が注目されています。細菌のもつDNA 切断酵素CRISPR-Cas9(注2)を応用したゲノム編集技術は、基礎研究から臨床応用に至る多岐にわたる生命科学分野において広く利用されています。今回、東京大学大学院理学系研究科の西増 弘志助教、濡木 理教授、金沢大学新学術創成研究機構の柴田 幹大准教授、金沢大学理工研究域バイオAFM先端研究センターの古寺 哲幸准教授、安藤 敏夫特任教授、名古屋大学大学院理学研究科の内橋 貴之教授らは、高速AFM(注3)を用いることにより、CRISPR-Cas9 がDNA を切断する一連の様子を動画として撮影することに成功しました。本研究結果は、CRISPR-Cas9 によるDNA 切断メカニズムの深い理解につながるとともにゲノム編集技術の高度化の基盤となることも期待されます。
内容
近年、生命の設計図であるゲノム情報を書き換える「ゲノム編集」と呼ばれる技術が脚光を浴びています。ゲノム編集は、生命科学の基礎研究から動植物の品種改良や疾患の治療にいたる幅広い分野において利用されている革新的な技術です。ゲノム編集にはCas9 と呼ばれるDNA切断酵素が用いられます。Cas9 はガイドRNA と結合し、ガイドRNA の一部(ガイド配列)と相補的なDNAを選択的に切断するはたらきをもちます(図1)。すなわち、Cas9 はDNA を切る「ハサミ」としてはたらく一方、ガイドRNA は「案内役」としてCas9 を標的となるDNAへと導きます。20 塩基のガイド配列は自由に設計し交換できるため、Cas9 と人為的に作製したRNA を用いることにより、ゲノムDNA の様々な部位を選択的に切断することが可能です。ゲノム編集技術では、Cas9 によって切断された部位が修復される過程において生じる塩基配列の変化を利用します。
これまでに本研究グループや海外の研究グループによってCRISPR-Cas9の結晶構造が決定され、DNA切断メカニズムの理解が進んできました。Cas9 単体、ガイドRNA と結合した状態(Cas9-RNA 複合体)、ガイドRNA および標的DNA と結合した状態(Cas9-RNA-DNA 複合体)の結晶構造の比較から、RNA やDNA の結合に伴い、Cas9 は構造を大きく変化させることが示唆されていました(図2)。しかし、結晶構造は分子のある一状態を捉えた「スナップショット」であるため、実際にCas9 がどのような構造変化を起こすのかは不明でした。
今回、本研究グループは高速AFMを用いることにより、CRISPR-Cas9 がはたらく一連の様子を動画撮影することに成功しました。高速AFMは、金沢大学が世界にさきがけて開発してきた顕微鏡技術で、水溶液中の生体分子をナノメートル(10 億分の1メートル)の空間分解能で、かつ、リアルタイムに撮影することができます。高速AFMを用いて、これまでに様々なタンパク質や生きた細胞のダイナミックな動きが明らかにされてきました。そこで、結晶構造から明らかになっている「スナップショット」に加え、水溶液中での「ダイナミクス」を明らかにすることにより、CRISPR-Cas9 のはたらく仕組みの深い理解を目指し研究を行いました。
まず、高速AFMを用いてCas9 単体を観察したところ、時間とともに次々にダイナミックに形を変える様子が捉えられました(図3)。これは、結晶構造では明らかになっていなかった予想外の発見でした。その一方、高速AFM 動画において、Cas9-RNA 複合体は、結晶構造と一致した安定な構造をとっていました(図4)。これらの結果から、Cas9 単体の柔軟な構造はRNA との結合に重要であること、および、RNA はCas9 の立体構造の安定化に貢献していることが示唆されました。次に、標的配列を1 つだけ含むDNA とCas9-RNA 複合体を混合し高速AFM観察をしたところ、Cas9-RNA 複合体はDNA と衝突を繰り返すことにより標的配列を見つけ出し、安定に結合する様子が明らかになりました(図5)。これまでCas9-RNA 複合体がどのようにDNA の標的配列を探索するのか議論されてきましたが、高速AFM 動画から、Cas9-RNA 複合体はDNA 上をスライドするのではなく、3 次元方向への拡散を利用したDNA への衝突により標的配列を探索することが直接的に示されました。さらに、DNA に結合したCas9-RNA 複合体を詳細に観察すると、DNA を切断する「ハサミ」としてはたらく部分(HNH ドメイン)が大きく揺らいだ構造をとることがわかりました。さらに、Cas9-RNA-DNA 複合体を高速AFM観察している間に、切断反応に必要なマグネシウムイオンを添加したところ、HNH ドメインがDNA の切断部位に移動したのち、切断されたDNA がCas9 から離れる様子を撮影することに成功しました(図6)。これまでに、生化学的解析や結晶構造解析、蛍光プローブを用いた1分子観察の結果から、DNA 切断の際にHNH ドメインが“動く”ことが示唆されていましたが、どのように動くのかは不明でした。したがって、今回の高速AFM動画は、Cas9 の「ハサミ」の動きをリアルスペースかつリアルタイムで可視化した画期的な研究成果といえます。
以上のように、Cas9 単体、Cas9-RNA 複合体、および、Cas9-RNA 複合体によるDNA の探索と切断といった一連の過程を撮影した高速AFM動画から、CRISPR-Cas9 によるDNA 切断のダイナミクスが明らかになりました(図7)。本研究により得られた動的な構造情報は、より高効率・高精度なゲノム編集ツールの開発の基盤となることが期待されます。
本研究は、日本学術振興会科学研究費助成事業、金沢大学新学術創成研究機構ユニット研究推進経費、花王芸術・科学財団花王科学奨励賞、ブレインサイエンス振興財団研究助成(研究代表者:柴田 幹大)、科学技術振興機構(JST) 戦略的創造研究推進事業 さきがけ「立体構造にもとづく次世代ゲノム編集ツールの創出」(研究者:西増 弘志)、科学技術振興機構(JST) 戦略的創造研究推進事業 さきがけ「新規高速原子間力顕微鏡で解き明かすミオシンV の化学-力学エネルギー変換機構」(研究者:古寺 哲幸)、CREST「ATP/GTP が駆動するタンパク質マシナリーの動的構造生命科学」(研究代表者:安藤 敏夫)、科学研究費助成事業、新学術領域「理論と実験の協奏による柔らかな分子系の機能の科学」、「生命システムにおける動的秩序形成と高次機能発現」(研究代表者:内橋 貴之)、文部科学省(2014 年度)・日本医療研究開発機構(AMED)(2015 年度以降)革新的バイオ医薬品創出基盤技術開発事業「新規CRISPR-Cas9システムセットの開発とその医療応用」(研究代表者:濡木 理)の一環として行われました。
添付資料
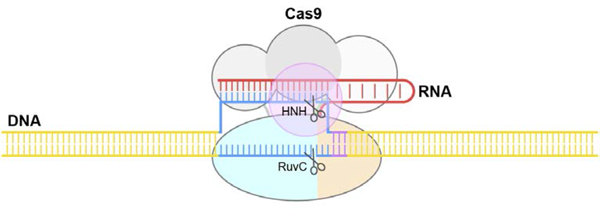
図1 CRISPR-Cas9 によるDNA 切断メカニズム
Cas9 はいくつかの部分(ドメイン)から構成される。HNH およびRuvC と呼ばれるドメインが「ハサミ」としてはたらき二本鎖DNA を切断する。
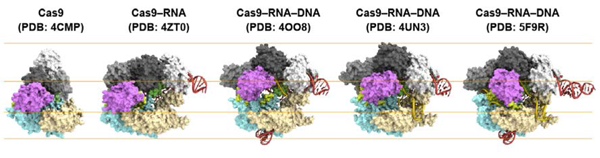
図2 CRISPR-Cas9 の結晶構造

図3 Cas9 単体の高速AFM動画

図4 Cas9-RNA 複合体の高速AFM動画
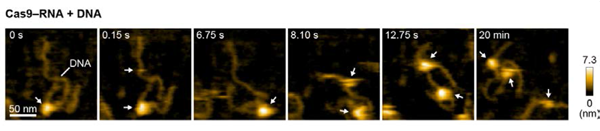
図5 Cas9-RNA 複合体によるDNA の探索

図6 Cas9-RNA 複合体によるDNA の切断
(a)DNA の切断部位から離れた状態のHNH ドメイン (b)切断部位に近い状態のHNH ドメイン
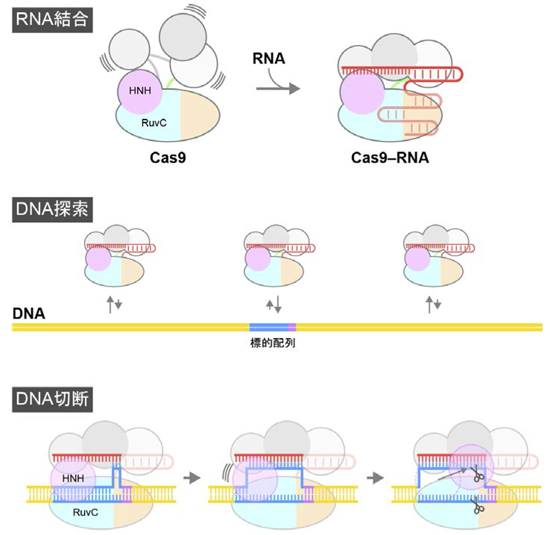
図7 CRISPR-Cas9 によるDNA 切断のダイナミクス
Cas9 はガイドRNA と結合しCas9-RNA 複合体を形成する。Cas9-RNA 複合体はDNA と衝突を繰り返すことにより、ガイド RNA と相補的な標的配列を見つけ出し強固に結合する。 Cas9-RNA 複合体が標的配列に結合すると、DNA の巻き戻しが起こり、HNHドメインはDNAの近傍に移動し、相補鎖DNA を切断する。一方、RuvCドメインは一本鎖となった非相補鎖DNAを切断する。
用語解説
掲載論文情報
- 論文タイトル
- Real-space and real-time dynamics of CRISPR-Cas9 visualized by high-speed atomic force microscopy
- 著者
- Mikihiro Shibata12,7,*, Hiroshi Nishimasu 3,4,7,*, Noriyuki Kodera2,4, Seiichi Hirano3, Toshio Ando2,6, Takayuki Uchihashi2,5,6,‡, and Osamu Nureki3,*
1.金沢大学新学術創成研究機構
2.金沢大学理工研究域バイオAFM先端研究センター 3.東京大学大学院理学系研究科
4.科学技術振興機構(JST)・さきがけ
5.金沢大学理工研究域数物科学系
6.科学技術振興機構(JST)・CREST
7.同等貢献*責任著者
‡現名古屋大学大学院理学研究科 - 掲載誌
- Nature Communications
- 掲載日
- 2017.11.10

