リソソーム制御が脳腫瘍治療のカギ!~アミノ酸バランスを活用した“抗がん剤ブースター療法”を開発~
金沢大学ナノ生命科学研究所(WPI-NanoLSI)/がん進展制御研究所の平尾敦教授、がん進展制御研究所のジン・ヨンウエイ博士研究員、小林昌彦助教、医薬保健研究域医学系の中田光俊教授、医薬保健研究域薬学系の荒川大准教授、ナノ生命科学研究所(WPI-NanoLSI)の新井敏教授らの研究グループは、東京大学医科学研究所、慶應義塾大学先端生命科学研究所、和歌山県立医科大学と共同で、悪性脳腫瘍の抗がん剤に対する耐性が「リソソーム」(※1)の働きによって引き起こされることを明らかにしました。また、アミノ酸のバランスを変えることでリソソームの機能が低下し、抗がん剤の効果が高まることも発見しました。
悪性脳腫瘍の一種である膠芽腫(グリオブラストーマ)は、手術、放射線治療、そして「テモゾロミド」(ここでは、TMZと略します)という抗がん剤で治療するのが一般的です。しかし、多くの患者さんは治療後に再発し、がんがさらに悪化してしまいます。そのため、治療が効かなくなる仕組みを解明し、新たな治療法を開発することが急務となっています。
今回の研究では、細胞内の「リソソーム」を制御する重要な因子「TFE3」(※2)がリソソームを活性化し、治療が効かなくなる原因となることを発見しました。さらに、アミノ酸の一種である「リシン」が、リソソームの機能維持に不可欠な役割を果たしていることも明らかになりました。このリシンの働きを阻害する低分子化合物(※3)を投与することで、アミノ酸のバランスを崩し、リソソームの機能を低下させることを確認しました。この結果は、抗がん剤の治療効果を飛躍的に向上させる「抗がん剤ブースター療法」の確立に向けた重要な成果といえます。将来的に、この成果を医療に応用することで、悪性脳腫瘍の治療成績の改善に貢献することが期待されます。
本研究成果は、2025年4月1日(英国時間)に英国科学誌『Nature Communications』に掲載されました。
【研究の背景】
タンパク質、糖、脂質、ビタミン、ミネラルなどの栄養素を摂取し、体内で代謝することは、私たちが生きる上で非常に重要です。これまでの研究で、これらの栄養素を感知する仕組みが、エネルギーの産生や消費のバランスを調整したり、エピジェネティクス(遺伝子の働きの調整)やレドックス(酸化還元)シグナルの伝達経路に影響を与えたりすることで、がん細胞の生存や増殖を強くコントロールしていることが分かってきました。
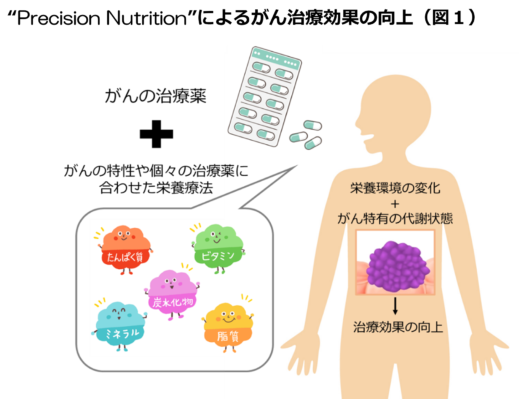
最近、こうしたがん特有の代謝状態に着目し、それぞれの弱点を狙った栄養療法が開発されつつあります。例えば、がんが必要とする栄養素を減らすことで、腫瘍の成長を抑える効果が確認されています。また、従来のがん治療と特定の栄養療法を組み合わせることで、治療効果が大きく向上する可能性も示されています。このようなアプローチは“Precision Nutrition”と呼ばれ(日本語では、「精密栄養」「個別化栄養」などと訳されます)、患者さんの状態に合わせた食事を設計し、治療効果を最大限に引き出しつつ、副作用を最小限に抑えることを目指しています(図1)。
本研究では、治療が効きにくい脳腫瘍の代謝的特性に着目し、治療の効果を高める栄養療法を開発することを目標に研究を進めました。
【研究成果の概要】
発見のポイント
1.リソソーム生合成調節因子TFE3は、脳腫瘍細胞の治療耐性の原因となる
2.アミノ酸「リシン」は、リソソーム機能に不可欠である
3.リシン・アルギニンバランスを崩すと抗がん剤の治療効果が高まる
ポイント1.リソソーム生合成調節因子TFE3は、脳腫瘍細胞の治療耐性の原因となる
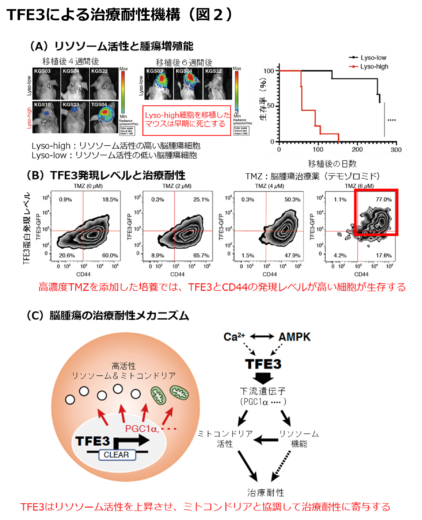
金沢大学と東京大学で確立された悪性膠芽腫細胞株を解析したところ、これらの細胞は正常な神経前駆細胞に比べてリソソームの活性が高いことが分かりました。さらに、リソソーム活性が高い腫瘍細胞ほど、酸素を使うミトコンドリアの活動が活発であり、特殊な代謝状態を持つことが明らかになりました。また、リソソーム活性が高い細胞ほど、生体内で腫瘍を増やす能力が強く、悪性度が高い性質を持つことも判明しました(図2A)。このことから、リソソーム活性は脳腫瘍の悪性度を示す重要な指標になると考えられます。
次に、リソソーム活性を制御する因子を調べた結果、リソソーム生合成を調節する「TFE3」というタンパク質が、治療耐性に深く関わっていることが分かりました(図2B)。さらに、TFE3はPGC1αなどの分子を介して、腫瘍細胞の特徴的な代謝を調整していることも明らかになりました(図2C)。
ポイント2.アミノ酸「リシン」は、リソソーム機能に不可欠である
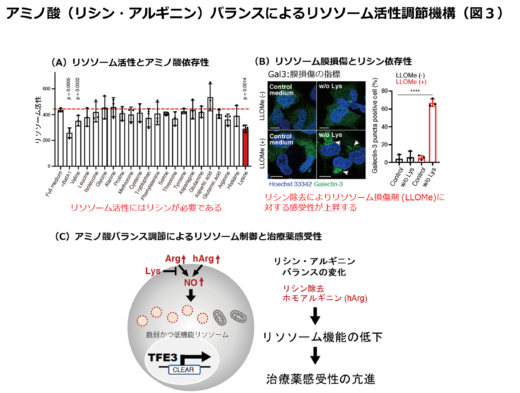
これらの結果をもとに、腫瘍細胞の代謝をさらに詳しく調べたところ、アミノ酸の動きが大きく変化していることが明らかになりました。そこで、培養液からアミノ酸を一つずつ取り除いて細胞を育て、リソソーム活性がどう変化するかを調べたところ、「リシン」というアミノ酸がリソソームの働きに不可欠であることが分かりました(図3AB)。
培養液中のリシン濃度を下げると、リソソームの機能が低下し、抗がん剤「テモゾロミド」に対する腫瘍細胞の感受性(治療効果)が高まることも確認されました。その仕組みとして、リシンがアルギニンを使った一酸化窒素の生成を抑えることで、腫瘍細胞をリソソームストレスから保護する役割を果たしていることが分かりました(図3C)。
以上より、細胞内のリシンとアルギニンのバランスを変えると、リソソームの機能が低下し、抗がん剤の効果が高まることを見出しました。
ポイント3.リシン・アルギニンバランスを崩すと抗がん剤の治療効果が高まる
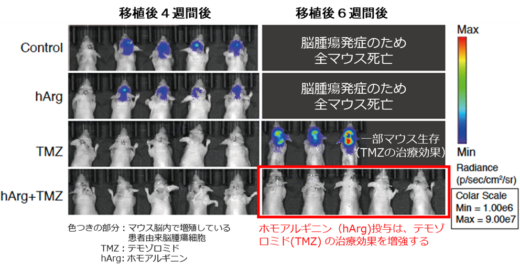
これらの知見をもとに、新しい治療法の開発を目指しました。リシンは体内で作れないため、食事から摂取する必要がある「必須アミノ酸」の一つです。そのため、まずはマウスモデルを用いて、リシンを含まない特別食により体内のリシンを制限する実験を行いました。しかし、この方法では体重が大きく減少する問題がありました。そこで、リシンを制限するのと同じ効果を持つ化合物を探した結果、「ホモアルギニン」という物質が、テモゾロミドの治療効果を高めることを発見しました(図3C)。ヒト脳腫瘍細胞を免疫不全マウスに移植したモデルで、ホモアルギニン単独では腫瘍に大きな効果はありませんでしたが、テモゾロミドと併用することで、抗腫瘍効果を高め、マウスの生存期間を延ばすことが確認されました(図4)。
これらの結果から、ホモアルギニンの投与は、テモゾロミドの治療効果を増強する「抗がん剤ブースター療法」として有効であることが確認できました。
【今後の展開】
今後は、TFE3を中心とした治療耐性の仕組みをさらに詳しく解析する必要があります。脳の組織内で、どのような代謝環境が治療耐性を作り出すのか、またどのような分子が影響を受けるのかを解明することで、がんの本質的な理解が進むと期待されます。
また、ホモアルギニンを医療に応用できる可能性や、それ以上に効果の高い化合物を見つけられるかについても検討が必要です。この際、抗がん効果だけでなく、安全性についてもしっかり確認することが重要です。
これらの取り組みを通じて、将来的に悪性脳腫瘍の治療成績や患者さんの予後を改善できるよう、研究開発を進めていきます。
用語解説
掲載論文情報
- 論文タイトル
- Lysine-arginine imbalance overcomes therapeutic tolerance governed by the transcription factor E3-lysosome axis in glioblastoma (リシンとアルギニンの不均衡を通じて、転写因子TFE3-リソソーム経路によって生じる膠芽腫の治療耐性を克服する)
- 著者
- Yongwei Jing, Masahiko Kobayashi, Mahmoud I. Shoulkamy, Meiqi Zhou, Ha Thi Vu, Hiroshi Arakawa, Hemragul Sabit, Sadahiro Iwabuchi, Cong Quang Vu, Atsuko Kasahara, Masaya Ueno, Yuko Tadokoro, Kenta Kurayoshi, Xi Chen, Yuhang Yan, Satoshi Arai, Shinichi Hashimoto, Tomoyoshi Soga, Tomoki Todo, Mitsutoshi Nakada, and Atsushi Hirao (荊泳瑋、小林昌彦、マハムド=イブラヒム・シャルカミ、周美琦、ハ・ティ・ヴ、荒川大、アムラ・サビット、岩淵禎弘、コン・クアン・ヴー、笠原敦子、上野将也、田所優子、倉吉健太、陳茜、鄢宇航、新井敏、橋本真一、曽我朋義、藤堂具紀、中田光俊、平尾敦)
- 掲載誌
- Nature Communications
- 掲載日
- 2025.04.01
- DOI
- 10.1038/s41467-025-56946-z
- URL
- https://www.nature.com/articles/s41467-025-56946-z