核の門番「核膜孔複合体」が関与するp53分解機構の阻害により脳悪性腫瘍の制御に成功!
金沢大学ナノ生命科学研究所/新学術創成研究機構の羽澤勝治准教授,ナノ生命科学研究所のリチャード・ウォング教授,医薬保健研究域医学系脳神経外科学の中田光俊教授らの研究グループは,脳悪性腫瘍である膠芽腫(こうがしゅ)(※1)において高い発現を示している核膜孔複合体(NPCs)(※2)の特定因子を抑制することにより,がん抑制タンパク質p53(※3)を正常化し,膠芽腫を制御できることを発見しました。
NPCsは,細胞核を出入りする全ての分子の輸送を制御する小さな孔(門)を形成し,細胞のさまざまな生命活動を支えています。本研究では,膠芽腫において,がん抑制遺伝子p53の発現を確実に抑え込む新たな機構が存在することを発見しました。膠芽腫細胞では,NPCsによる選択的な核外搬出システムとタンパク質分解経路を組み合わせた,高次タンパク質分解機構が確立され,効率よくp53が分解されていることを明らかにしました。このp53分解機構の制御により,膠芽腫の進展が阻害されました。
これらの知見は将来,膠芽腫における新たな治療法の確立に役立つことが期待されます。
本研究成果は,2023年8月7日10時(米国東部時間)に米国科学誌『Cell Reports』のオンライン版に掲載されました。
研究の背景
細胞の核で生成される生命情報は,核膜孔複合体(NPCs)を介して細胞質に移動します。34種類のタンパク質で構成されるNPCsは,核-細胞質間を結ぶ唯一の輸送孔を形成し,特定の条件を満たす分子のみが核を出入りできる選択的輸送環境を構築しています。核内に存在するタンパク質が核外へ輸送する過程では,XPO1(※4)がタンパク質を認識し,NPCsまでエスコートします。このNPCsによる選択的な分子輸送システムは,細胞増殖・分化,ストレス応答などさまざまな基本生命現象を支えています。近年,がんなどの難治性疾患においてNPCsの構造・機能変容が報告されており,がんにおけるNPCsの役割を明らかにすることは,新たながんの治療法につながる重要な課題です。
p53は,がんの発生や進行を抑制する重要なタンパク質であり,膠芽腫においてその機能が抑制されています。細胞内の主要なタンパク質分解経路であるユビキチン化が,p53を速やかに分解することは知られていましたが,さまざまな分子で溢れている細胞内空間で,p53を効率よく分解する仕組みについては不明でした。
研究成果の概要
本研究では,膠芽腫におけるNPCsの変容と機能を明らかにすることを目的として開始されました。結果,膠芽腫ではNPCsによる選択的な核外搬出システムとタンパク質分解経路を組み合わせた,高次タンパク質分解機構が存在し,効率よくp53を分解していることが分かりました。
膠芽腫のゲノム解析より,NPCs構造の形成と安定性に重要な遺伝子NUP107およびp53ユビキチン化を促進する遺伝子MDM2で,過剰発現を引き起こすゲノム異常が併発していました。そのため,これらの膠芽腫では,過剰発現したNUP107とMDM2が協調的に機能することで,p53分解機構を活性化する可能性が想定されました。事実,NUP107の発現を抑制した細胞核では,構造が未熟なNPCsが増加した結果,p53が安定化し,膠芽腫細胞の増殖は抑制されました。また,XPO1の機能阻害により,p53が安定化したことから,膠芽腫細胞におけるp53分解機構は,XPO1とNPCsによる核外搬出システムに依存することが分かりました。重要なことに,ユビキチン化されたp53を分解する装置(26Sプロテアソーム)が,NPCsと結合していることが超解像度顕微鏡で明らかとなりました。このことは,膠芽腫においてXPO1によるNPCsへの選択的な運搬と,26Sプロテアソームを組み合わせたp53分解機構が,悪性化に関与していることを示しています。
今後の展開
核構造に結びついたp53分解機構を制御することで,p53を再活性化する新たな創薬開発や治療戦略につながることが期待されます。
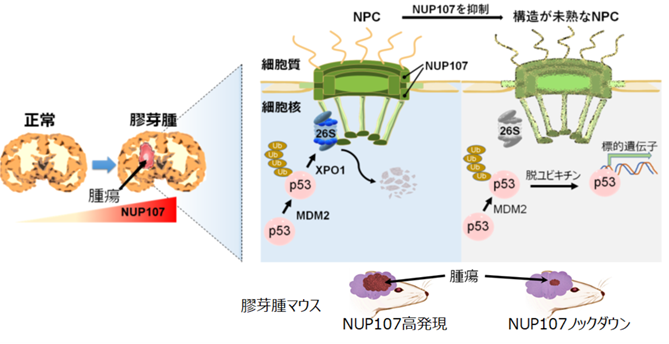
図1:膠芽腫における核外搬出システムを活用したp53分解機構
XPO1とNPCsによる選択的な核外搬出システムとタンパク質分解装置26Sプロテアソームを組み合わせた,高次タンパク質分解機構。MDM2により分解シグナルが付加されたp53を確実に分解するために,膠芽腫細胞株は核外搬出機構を活用し,NPCsに結合した26SプロテアソームへXPO1が選択的に運搬するシステムを確立している。
用語解説
掲載論文情報
- 論文タイトル
- Nuclear transport surveillance of p53 by nuclear pores in glioblastoma(膠芽腫における核膜孔によるp53の核輸送監視)
- 著者
- Dini Kurnia Ikliptikawati, Nozomi Hirai, Kei Makiyama, Hemragul Sabit, Masashi Kinoshita, Koki Matsumoto, Keesiang Lim, Makiko Meguro-Horike, Shin-ichi Horike, Masaharu Hazawa, Mitsutoshi Nakada, Richard W. Wong(ディニ クルニア・イクリプティカワティ, 平井 希, 牧山 桂, 淑瑠 へムラサビット, 木下 雅史, 松本 晃希, キイシヤン・リン, 目黒 牧子, 堀家 慎一, 羽澤勝治#, 中田 光俊#,リチャード・ウォング#)#:共同責任著者
- 掲載誌
- Cell Reports
- 掲載日
- 2023.08.07
- DOI
- 10.1016/j.celrep.2023.112882
- URL
- https://www.cell.com/cell-reports/fulltext/S2211-1247(23)00893-8

