多くのがんの治療や診断への応用が期待される 新規「中分子薬剤」の開発
金沢大学医薬保健研究域薬学系の淵上剛志准教授,ナノ生命科学研究所の宮成悠介准教授,新学術創成研究機構の小川数馬教授,長崎大学医歯薬学総合研究科の野﨑伊織大学院生らの共同研究グループは,多くのがん診断・がん治療医薬品への応用が期待される,これまでに報告例のない新しいタイプの中分子薬剤の開発に成功しました。
Survivin(※1)は,ほとんどの正常細胞では検出されませんが,多くのがん細胞で高発現しているタンパク質で,がんの診断薬や治療剤の有望な標的として期待されています。しかしながら,現在までに医療の現場において,survivinを標的とする医薬品の実用化には至っていません。
今回,本研究グループは,独自の分子設計にてsurvivinへ強い結合性を示し,がん細胞の検出や生体内のがん細胞を退縮させることができる新しい中分子化合物(※2)を見出しました。本研究をさらに発展させることにより,あらゆるがんの診断や治療へ適応できる医薬品の開発につながることが期待されます。
本研究成果は,2022年11月1日アメリカ化学会が出版する国際化学誌『Bioconjugate Chemistry』のオンライン版に掲載されました。
研究の背景
Survivinは,肝がん,膵がん,肺がんなどのさまざまながん細胞において高発現している一方,分化後の正常組織にはほとんど発現が見られません。このため,がんの診断薬や治療剤の有望な標的として,これまでに低分子や核酸を母体とした医薬品候補化合物が開発されてきましたが,現在までに臨床にて使用される医薬品の開発には至っておりません。従って,これまでにない新たなタイプのsurvivin標的分子の創出が望まれています。
研究成果の概要
Survivinは,細胞内でINCENP,Borealinと呼ばれるタンパク質と強固なヘリックス束から成る染色体パッセンジャー複合体(※3) を形成します。そこでこのタンパク質複合体に注目してそれらの結合情報を抽出し,独自の分子設計にてsurvivinを標的とした中分子化合物 (※2) (ペプチド誘導体) を開発しました。その結果,Bor65-75というsurvivinに高親和性を示す新規ペプチド誘導体を見出しました。そのペプチド分子を蛍光標識した誘導体 (FITC-Bor65-75) はsurvivinの発現に一致した細胞内集積を示したことから(図1),高感度かつ高い選択性にてがん細胞を見つけることのできる診断薬へと展開できる可能性が示されました。Survivinは細胞内に存在するタンパク質であることから,細胞膜を透過できるペプチド分子 (r9-Bor65-75) へと誘導化したところ,がん細胞への強い増殖抑制効果を示した一方,正常細胞には弱い殺傷効果しか示しませんでした(図2)。また,r9-Bor65-75はsurvivinタンパク質自体の分解は引き起こしませんでしたが,強いアポトーシス誘発効果を有することが見出され,このペプチド分子はsurvivinの機能を阻害することにより抗がん活性を示すことが示唆されました。次いで,膵臓がん細胞を移植したマウスへの治療効果を調べたところ,r9-Bor65-75を投与した腫瘍組織は,注射液のみを投与した腫瘍組織に比べて有意な退縮効果が認められました(図3)。一方で,体重減少などの顕著な副作用は確認されませんでした。以上の結果より,r9-Bor65-75などのsurvivinを標的とした中分子化合物が,がんの診断薬や治療薬へと展開できる可能性が示されました。
今後の展望
Survivinは初期のがん組織にも発現が見られることから,PETなどの核医学画像診断のための放射性薬剤への展開が期待されます。また,survivinは化学療法や放射線治療への抵抗性を示すことが報告されています。そこで,他の抗がん剤との併用療法やα線放出核種などを導入した核医学治療薬剤への応用などにより,相乗的な抗がん活性が期待されます。また,survivinは血液中の循環腫瘍細胞からも検出されることから,高感度ながんの血液診断の標的タンパク質としても有望と考えられます。現在、創発的研究支援事業(JST)にて,がんの血液診断から治療までを一貫して行える医療技術創出を目指して研究を進めており,本研究で見出された中分子化合物をさらに応用することにより,そのような技術の実用化につながることが期待されます。
研究資金
本研究は,日本学術振興会 科研費(17J11488,21H02867,21H04765,22H03015),科学技術振興機構(JST) 創発的研究支援事業(FOREST, JPMJFR200V),武田科学振興財団,小林がん学術振興会,テルモ生命科学振興財団などの支援を受けて実施されました。
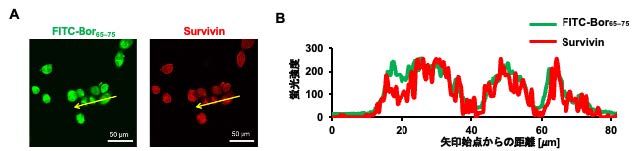
図1 FITC-Bor65-75 の細胞内集積
(A) 細胞内への蛍光標識ペプチド誘導体 FITC-Bor65-75の集積 (緑) とsurvivinの発現部位 (赤)
(B) (A)の画像矢印領域の蛍光強度解析
FITC-Bor65-75の集積部位はsurvivinの発現部位と類似していることから,
このペプチド分子がsurvivinを高選択的に認識していることが示唆された。
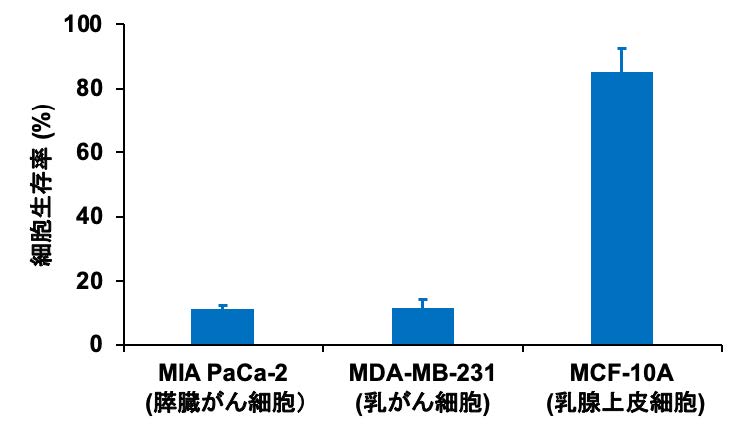
図2 r9-Bor65-75 (10 μM) の細胞殺傷効果
ペプチド誘導体r9-Bor65-75は,がん細胞であるMIA PaCa-2細胞やMDA-MB-231
細胞へ強い細胞殺傷効果を示す一方で,正常細胞のMCF-10A細胞へは非常に
弱い毒性しか示さなかった。
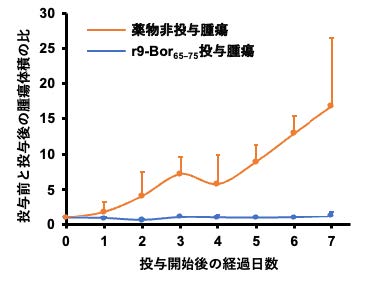
図3 r9-Bor65-75の腫瘍モデルマウスへの抗腫瘍活性評価
両肩に膵臓がん細胞 (MIA PaCa-2) を移植したマウスの右肩にr9-Bor65–75 (10 mg/kg) を,左肩に注射液のみを24時間後ごとに7日間投与した後の腫瘍体積変化。
r9-Bor65-75を投与した腫瘍組織では薬物を投与していない腫瘍組織に比べて大幅な腫瘍組織の退縮効果が見られた。
用語解説
掲載論文情報
- 論文タイトル
- Borealin-derived peptides as survivin targeting cancer imaging and therapeutic agents
- 著者
- Iori Nozaki, Natsumi Ishikawa, Yusuke Miyanari, Kazuma Ogawa, Ayako Tagawa, Sakura Yoshida, Masayuki Munekane, Kenji Mishiro, Akira Toriba, Morio Nakayama, Takeshi Fuchigami
- 掲載誌
- Bioconjugate Chemistry
- 掲載日
- 2022.11.01
- DOI
- 10.1021/acs.bioconjchem.2c00398
- URL
- https://doi.org/10.1021/acs.bioconjchem.2c00398

