創薬と次世代薬物療法の創出を目指した薬物代謝と毒性学研究
薬物応答性と医薬品毒性の個人差を規定する薬物代謝酵素の役割

中島美紀、金沢大学ナノ生命科学研究所 教授・主任研究者
医薬品(薬)は私たちの生活に広く普及している。薬のほとんどは化学物質であり、糖尿病やがん、頭痛や心臓の機能不全など、様々な病気を治療・予防するために用いられている。
私たちの体は、異物が入ってくると体を守るためにその異物を排除しようとするが、薬に対しても同じように反応する。一般的に、薬の錠剤やカプセルは胃の中で溶け、その成分は腸から吸収されて肝臓に運ばれる。肝臓でその成分の一部は解毒され、残りは血流にのって標的組織に到達して作用し、排泄される仕組みだ。
「薬が体内に入ると、4つの過程をたどります。まず、体内に吸収(Absorption)され、血流にのって全身に分布(Distribution)し、肝臓などで代謝(Metabolism)され、最後は体外に排泄(Excretion)されます。この過程はそれぞれの頭文字をとって ADME(アドメ)と呼ばれます」と中島美紀教授は説明する。この研究分野は薬物動態学と呼ばれており、中島教授は主に薬物代謝を研究している。「私は、創薬と薬物療法の最適化のために、薬物応答性および医薬品毒性発症における個人差や個人内変動、ならびに薬物間相互作用を制御するメカニズムを解明したいと思っています。そのためには、薬が体内でどのように反応するかを理解することが重要なのです」。図1は、薬が投与されてからADMEの過程を介して、どのように血中濃度が変化するかを示している。
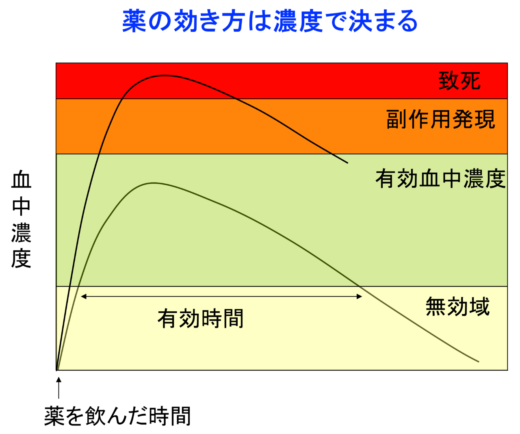
図1.体内における薬の血中濃度の経時変化
ここで重要なのは、肝臓が2つの代謝プロセスによって、化合物の構造を変化させる点である。第I相代謝反応では脂溶性の薬物を水溶性の化合物に変換し、より排出されやすくし、時に、反応性の高い代謝物(薬理活性体または毒性の原因となる反応性代謝物)を産生する。第II相代謝反応では、極性の高い官能基を抱合することで化合物の水溶性をさらに高め、解毒する。
「薬物代謝酵素は、同じ薬を同じ量服用しても認められる薬効や医薬品毒性の個人差を規定する鍵要因であるだけでなく、喫煙や飲酒、食事で摂取した低分子化合物や環境汚染物質など、あらゆる生体外異物の解毒代謝にも重要な役割を担っているため、私たちは、第I相代謝酵素であるシトクロムP450を中心に、薬物代謝酵素の研究をしています。」と中島教授は説明する。
近年、中島教授らはヒトCYP2A6(P450の一種)がmicroRNA(miRNA)によって制御されていることを発見した。「私たちは、CYP2A6がmiR-126*によって転写後調節を受けること、また、CYP2A6の偽遺伝子産物(遺伝子が複製を繰り返すうちに、突然変異によりタンパク質をつくる機能を失ったもの)であるCYP2A7もmiR-126*によって制御され、その結果CYP2A7がmiR-126*結合に対して競合的に働くことでCYP2A6の発現量に影響を与えることを発見しました。CYP2A6は抗がん薬を代謝する酵素ですし、またたばこに含まれる前発がん物質を発がん物質に変換する酵素であるので、私たちの研究は抗がん薬の開発や、たばこと発がんの関係を解明するための重要な手がかりとなります」[1]。
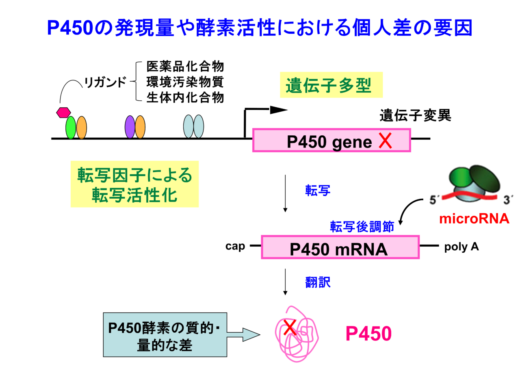
図2. ヒトP450酵素の発現量とその機能に個人差をもたらす要因
ナノ生命科学研究所において、中島教授は、原子間力顕微鏡(AFM)技術を活用して、脂質膜上でのP450とP450還元酵素の相互作用と、それに関係するプロセスをモニタリングする。さらに、医薬品毒性の原因となる反応性代謝物を捕捉可能な超分子の開発や、医薬品毒性とエクソソームの関わりについて分析することも視野にいれている。
研究ハイライト
『Pharmacology & Therapeutics』[2] に発表された2018年の論文において、中島教授らは、抗がん薬の標的分子におけるA-to-I RNA編集が薬物応答性に影響を及ぼしていることを証明した研究結果を報告している。
また、中島教授らはmicroRNAが薬物代謝酵素の発現を制御することで、薬物応答性や発がん、生体内化合物のホメオスタシスの調節に関わっていることを世界で初めて報告し、国際的に高く評価されている。
参考文献
[1] M. Nakano et al, “CYP2A7 pseudogene transcript affects CYP2A6 expression in human liver by acting as a decoy for miR-126*”, Drug Metab Dispos, 43, 703-712 (2015).
doi: 10.1124/dmd.115.063255
[2] M. Nakano and M. Nakajima, “Significance of A-to-I RNA editing of transcripts modulating pharmacokinetics and pharmacodynamics”, Pharmacology & Therapeutics 181, 13-21 (2018).
doi.org/10.1016/j.pharmthera.2017.07.003
[3] Y. Tsuchiya et al, “MicroRNA regulates the expression of human cytochrome P450 1B1”, Cancer Res 66, 9090-9098, (2006).
doi:10.1158/0008-5472.CAN-06-1403

