肺がん細胞が分子標的薬から生き延びるメカニズムを解明!
- 分子標的薬(※1)にさらされた肺がん細胞がAXL(アクセル)(※2)というタンパク質を使って生き延びることを初めて明らかにした。
- がんの分子標的薬は,効果があった場合でも腫瘍の一部が生き残り,再発することが問題だったが,EGFR変異肺がん(※3)において,分子標的薬にさらされた腫瘍細胞の一部が生き残るメカニズムを解明した。
- 動物実験でAXL阻害薬と分子標的薬の併用で肺がん細胞をほぼ死滅させ,再発を著明に遅らせることにも成功した。
- 将来,肺がんを根治させる治療につながるものと期待される。
概要
金沢大学がん進展制御研究所/ナノ生命科学研究所の矢野聖二教授,京都府立医科大学の山田忠明講師,長崎大学病院の谷口寛和助教らの共同研究グループは,分子標的薬(※1)にさらされた肺がん細胞がAXL(アクセル)(※2)というタンパク質を使って生き延びることを初めて明らかにしました。
がんの分子標的薬は,効果があった場合でも腫瘍の一部が生き残り,再発することが問題でした。
本研究グループは,EGFR変異肺がん(※3)において,分子標的薬にさらされた腫瘍細胞の一部が生き残るメカニズムを解明しました。さらに,動物実験でAXL阻害薬と分子標的薬の併用で肺がん細胞をほぼ死滅させ,再発を著明に遅らせることにも成功しました。
本研究成果は,将来,肺がんを根治させる治療につながるものと期待されます。
本研究成果は,2019年1月16日10時(英国時間)に英国科学誌「Nature Communications」のオンライン版に掲載されました。
研究の背景
がんの分子標的薬は,高い確率で奏効するものの腫瘍の一部が消えきらずに生き残り,残存した腫瘍が薬に耐性を獲得して大きくなり再発することが問題でした(図1)。従来の研究では,がんが分子標的薬に耐性化する原因を見つけ,耐性腫瘍にも効く新世代分子標的薬が作られてきましたが,新世代分子標的薬に対しても耐性が起こるため,耐性とのいたちごっこが続いています。
研究成果の概要
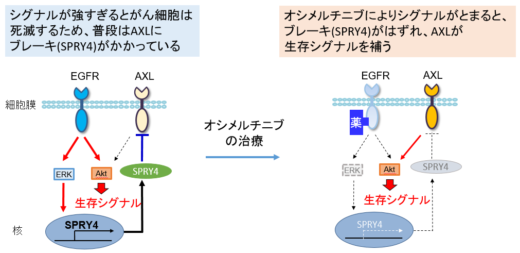
本研究では,EGFR変異肺がんにおいて,新世代分子標的薬オシメルチニブ(※4)にさらされた腫瘍細胞の一部が生き残るメカニズムを解明しました(図2)。
がん細胞は,変異したEGFRタンパク質からの生存シグナルにより増殖していますが,そのシグナルがあまりにも強すぎると逆に死んでしまうため,AXL(アクセル)というタンパク質にブレーキ(SPRY4)(※5)がかけられています。
しかし,新世代分子標的薬オシメルチニブにさらされた時には,EGFRタンパク質からの生存シグナルが抑制されることでSPRY4によるブレーキがはずれるため,AXLが活性化されてがん細胞が生き延びるための生存シグナルを補うことで一部のがん細胞がパーシスター(抵抗性細胞)(※6)として生き残ることを明らかにしました(図3)。
さらに,動物実験などでAXL阻害薬を新世代分子標的薬と併用すると,がん細胞をほぼ死滅させ再発を著明に遅らせることを発見しました。
今後の展開
本研究成果により,がん細胞がAXLというタンパク質を高発現している患者に,治療当初から分子標的薬とAXL阻害薬を併用した治療をすることで,腫瘍を消しきり,根治あるいは再発までの期間を著明に延ばせることが期待されます。
今後は,効果や副作用の面から最適なAXL阻害薬を選び出し,分子標的薬と併用する臨床試験を行いたいと考えています。
本研究は,国立研究開発法人日本医療研究開発機構(AMED)次世代がん医療創生研究事業「MAPKシグナル抑制が誘導するフィードバック機構の不均一性解明と制御に基づくKRAS/BRAF変異腫瘍に対する新規治療開発」(研究代表者 矢野聖二),日本学術振興会科学研究費助成事業,小林がん学術振興会研究助成,金沢大学がん進展制御研究所共同研究費,日本肺癌学会研究助成の支援を受けて実施されました。
【図1】分子標的薬は一旦効くが,腫瘍の一部が残存し再発の原因になる
黄色い丸は肺がんの腫瘍を示す。
【図2】AXLを発現しているがん細胞がパーシスターとして生き残る
【図3】オシメルチニブにより生存シグナルがオフになると,ブレーキがはずれAXLが生存シグナルを補う
用語解説
掲載論文情報
- 論文タイトル
- AXL confers intrinsic resistance to osimertinib and advances the emergence of tolerant cells
(AXLはオシメルチニブに対する初期耐性を惹起し抵抗性細胞の発生を促進する) - 著者
- Hirokazu Taniguchi, Tadaaki Yamada, Rong Wang, Keiko Tanimura, Yuta Adachi, Akihiro Nishiyama, Azusa Tanimoto, Shinji Takeuchi, Luiz H. Araujo, Mariana Boroni, Akihiro Yoshimura, Shinsuke Shiotsu, Isao Matsumoto, Satoshi Watanabe, Toshiaki Kikuchi, Satoru Miura, Hiroshi Tanaka, Takeshi Kitazaki, Hiroyuki Yamaguchi, Hiroshi Mukae, Junji Uchino, Hisanori Uehara, Koichi Takayama, Seiji Yano
(谷口寛和,山田忠明,王融,谷村恵子,足立雄太,西山明宏,谷本梓,竹内伸司,ARAUJO Luiz H,BORONI Mariana,吉村彰紘,塩津伸介,松本勲,渡部聡,菊池利明,三浦理,田中洋史,北崎健,山口博之,迎寛,内野順治,上原久典,高山浩一,矢野聖二) - 掲載誌
- Nature Communications
- 掲載日
- 2019.01.16
- DOI
- 10.1038/s41467-018-08074-0
- URL
- http://doi.org/10.1038/s41467-018-08074-0