受容体の活性化サイクルの網羅的可視化 ―時間分解構造解析により明らかになったGPCRのGタンパク質選択性と 2つのGタンパク質活性化経路―
発表のポイント
- クライオ電子顕微鏡(cryo-EM)を用いた単粒子構造解析によりNTSR1が多様なGタンパク質を識別し、活性化するメカニズムを解明
- GDP/GTPを添加したサンプルによる時間分解cryo-EM手法を用いて、20を超える構造を決定しNTSR1によるGiタンパク質活性化サイクルの全貌を可視化
- NTSR1はGi/oタンパク質と従来知られていた複合体状態(C状態)とは異なる状態(NC状態)を取り、NC状態からのGタンパク質の解離はC状態からの解離と全く異なる速度や反応経路で進行することを解明
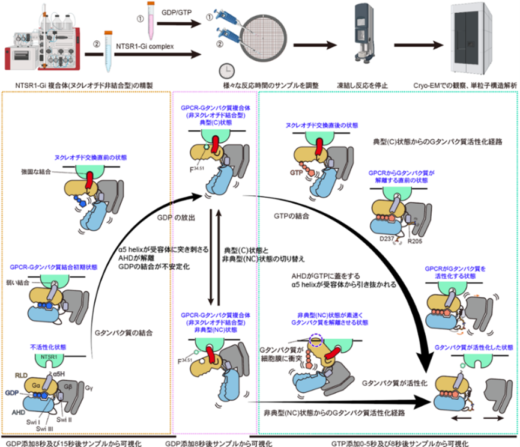
本研究の概略図
概要
東京大学先端科学技術研究センターの加藤英明教授と、京都大学大学院薬学研究科の井上飛鳥教授、明治大学理工学部の光武亜代理准教授、京都大学大学院生命科学研究科の角野歩准教授らによる研究グループは、ヒトの生理機能調節に深く関わり、創薬上重要な標的でもあるGタンパク質共役型受容体(GPCR)(※1)について、そのGタンパク質(※2)活性化メカニズムの詳細を明らかにしました。
細胞の表面には、ホルモンや神経伝達物質など外からの合図を受け取る「受容体」が並んでいます。なかでもGPCRは、痛み・血圧・食欲・精神機能など多様な生理機能を調節しており、現在使われる医薬品の多くがこのGPCRを標的としています。GPCRが合図を受けると、細胞内のGタンパク質がGPCRと結合し、Gタンパク質はヌクレオチド(※3)であるGDP結合時の“OFF”状態から、GTP結合時の“ON”状態へと切り替わります。その後、Gタンパク質は受容体から離れて別のタンパク質の活性化を制御することで、細胞外の情報を細胞内へと伝達していきます。ところが、GPCRがGタンパク質を認識し、活性化する一連の流れは、ミリ秒〜秒という非常に短い時間スケールで進むため、その過程において何が起きているのか、分子レベルでの詳細は十分に解明されていませんでした。
私たちは神経ペプチド「ニューロテンシン」の受容体であるNTSR1(※4)をモデルにこの課題に取り組みました。クライオ電子顕微鏡(cryo-EM)(※5)を用いた時間分解解析(※6)という手法を利用してNTSR1からGタンパク質が解離する過程をパラパラ漫画のように撮影・解析することで、GDPやGTPが結合する順番や、Gタンパク質内部に存在する“ふた”の開閉、受容体からの離脱が連動して起こる仕組みなどが次々に明らかになりました。さらに、高速原子間力顕微鏡や分子動力学シミュレーションといった手法も組み合わせることにより、NTSR1がGタンパク質と形成する、これまで存在は知られていたものの役割が不明だった「非典型(NC)状態(※7)」は、典型的な状態(C状態)とは別の活性化経路を持ち、C状態よりも素速くGタンパク質を活性化することを明らかにしました。
本研究成果は、2026年3月11日(英国標準時)に英国科学誌「Nature」のオンライン版に掲載されました。
発表内容
<研究の背景>
私たちの体は、外から来るさまざまな合図を「受容体」で受け取り、細胞の中に伝えて働きを変えています。GPCRはその代表で、におい・視覚・心拍・血圧・痛み・精神機能など幅広い生命現象に関わります。そのため、医療現場で使われる薬の多くがGPCRを標的にしています。GPCRが合図を受け取ったとき、細胞内で最初に動き出すのがGタンパク質です。Gタンパク質はGDPを結合していると休眠状態(OFF)で、GPCRに触れるとGDPが外れ、代わりにGTPが結合して作動状態(ON)になります。作動したGタンパク質は受容体から離れ、次の反応を進め、やがてGTPを分解して元に戻ります。つまり、GDPとGTPの“入れ替え”が、情報伝達の出発点です。
しかし、この活性化サイクルは非常に速く、途中の状態は不安定です。近年、cryo-EMによりGPCRとGタンパク質の複合体構造が多数明らかになってきましたが、多くはヌクレオチド(GDP/GTP)が外れた状態を中心とした反応の一場面のみに限られていました。そのため、GDP/GTPがどの順番で結合し、どの瞬間に受容体から離れるのかといった “動きの順序”を網羅的に追うことは、GPCRの生物学的な理解、ひいてはGPCRに対する創薬戦略への課題として残されたままでした。またNTSR1では、「典型(C)状態」に加え、「非典型(NC)状態」が報告されていたものの、実際に細胞内で働くのか、どんな役割をもつのかは不明でした。
さらに、GPCRがどの種類のGタンパク質を動かすかによって、同じ薬でも「治療効果」と「望ましくない作用」が分かれることがあります。たとえば痒みを抑える一方で眠気が出る、といった現象は、GPCRが活性化するGタンパク質の種類により切り替わります。したがって、副作用のない薬剤を開発する上で、スイッチが入る瞬間から切れる瞬間までの“反応の動画”を手に入れ、GPCRがそれぞれのGタンパク質を切り分けて活性化する仕組みを包括的に理解することは非常に強力な武器となります。
<研究の内容>
我々はNTSR1とGタンパク質(Go, Gq)を精製し、まずヌクレオチドが外れた複合体を作りました。これらのタンパク質を電子顕微鏡観察用の薄い膜(グリッド(※8))上に塗布し、cryo-EMを用いて観察し、その画像を解析しました。これらの構造からはNTSR1が異なるGタンパク質を見極めるために形を変えており、GPCRが特定のGタンパク質を選択する仕組みが明らかになりました。さらに、NTSR1とGタンパク質(Gi)からなる複合体を調整し、グリッド上でGTPを加えた後一定時間ごとに瞬間凍結しcryo-EMで観察しました。さらには、この複合体にGDPを加えることでGPCRの反応を巻き戻し、逆説的にGPCRにGタンパク質が結合する過程を観察しました。これらのサンプルから“時間の違う標本”を多数集めることで、反応の途中に現れる20以上の連続した写真を取得し、活性化サイクルのほぼ全貌を可視化することに成功しました。
特に、典型的な結合様式(C状態)において、Gタンパク質のα5ヘリックス(※9)部位とGタンパク質内部の“ふた”であるαヘリカルドメイン(AHD)(※10)が連動して動いており、これによりGDP/GTPの交換が生じることが明らかになりました(図1A-B)。具体的には、GDP/GTPがGタンパク質に結合する際に、まずリン酸側が結合ポケットに入り、その後塩基(グアニン)がポケットに収まること、GDP/GTPの結合と“ふた”の閉鎖がα5ヘリックスの離脱の引き金になることを示しました。さらに、GTPがGDPにはない3つ目のリン酸基を用いてGαとGβγを解離させる様子を捉えることにも成功しました(図1C)。
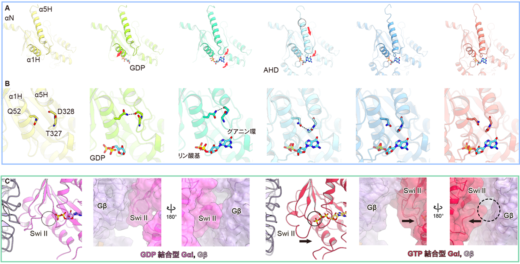
図1: ヌクレオチドの交換反応とGタンパク質が活性化するメカニズム
A: ヌクレオチドの結合からAHDの開閉、α5 helix(α5H)の引き抜きまでを可視化したもの。まずリン酸基がα1Hの近傍に結合し、その後グアニン環がポケットに結合する。その後、AHDがGDPを包み込むように“ふた”をし、α5HがGDP側に引き寄せられるように動く。赤矢印は直前のスナップショットからの動きを示している。
B: Aの拡大図。α5 helixの動きと連動するようにQ52が首振り運動をしていることが判明した。
C: GDP結合状態(左)とGTP結合状態(右)におけるGαとGβの相互作用界面の比較。GTPの持つ3個目のリン酸基がSwitch II loop(Swi II)をGαi側に引き寄せることで、GαiとGβの相互作用が弱くなっていることがわかる。
さらに重要な発見として、我々は、これまで役割が不明だった非典型(NC)状態はGタンパク質を直接活性化可能な状態であることを機能解析(※11)により明らかにし(図2A)、非典型(NC)状態はGDPやGTPに応答可能であり、典型(C)状態よりも反応性の高い機能的な状態であることを同定しました。特に、NC状態では“ふた”の閉鎖に依存しないユニークな仕組みでGタンパク質を活性化しており、Gタンパク質の一部が脂質膜(※12)に衝突することで「てこの原理」のような仕組みを通じてGタンパク質を活性化させるという、新規のメカニズムを見出すことに成功しました(図2B-C)。本研究からは、GPCRがGタンパク質を識別するメカニズムの解明のみならず、GPCRの反応サイクルのほぼ全貌が可視化され、さらにはこのような網羅的解析の結果として、非典型(NC)状態の機能性とそのユニークな活性化機構が明らかになりました。
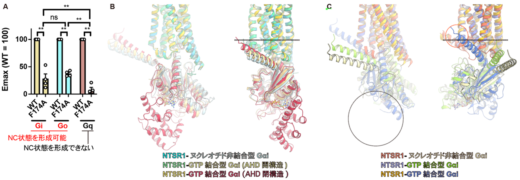
図2: 非典型(NC)状態はGタンパク質を活性化する機能的な状態である
A: F174A変異を導入したNTSRIは典型(C)状態からの活性を消滅させる一方で、非典型(NC)状態は活性能を維持する
B: 典型(C)状態からGタンパク質が活性化される際に観測された反応中間体
C: 非典型(NC)状態からGタンパク質が活性化される際に観測された反応中間体。AHDが閉じることなくGタンパク質がNTSR1から引き抜かれている。
<今後の展望>
今後は、NTSR1以外のGPCRや、Gi以外のGタンパク質でも同様の時間分解構造解析を展開し、「GPCRがどの経路を選ぶか」を決める分子要因を比較します。また、病気に関わる変異がサイクルのどこで滞るのかを可視化し、弱点となる中間状態を狙った新薬の創生を目指すとともに、今回得られた「反応の映画」を基準にGPCRサイクルの進み方を“ちょうどよく調整する”新しい治療薬を開発するための技術基盤の創出を目指します。
発表者・研究者等情報
東京大学 先端科学技術研究センター
小林 和弘(特任研究員)
川上 耕季(特任研究員、日本学術振興会特別研究員-PD)
加藤 英明(教授)<兼:大学院理学系研究科>
明治大学 理工学部
横井 駿(大学院博士後期課程学生(研究当時))
<現所属:筑波大学高等研究院 国際統合睡眠医科学研究機構・研究員>
光武 亜代理(准教授)
京都大学
大学院薬学研究科
井上 飛鳥(教授)<兼:東北大学 大学院薬学研究科・教授>
大学院生命科学研究科
角野 歩(准教授)<兼:金沢大学ナノ生命科学研究所(WPI-NanoLSI)/新学術創成研究機構(研究当時)>
炭竈 享司(特定講師)<兼:金沢大学ナノ生命科学研究所(WPI-NanoLSI)>
用語解説
掲載論文情報
- 論文タイトル
- The dynamic basis of G-protein recognition and activation by a GPCR
- 著者
- Kazuhiro Kobayashi, Kouki Kawakami, Toshiki E. Matsui, Shun Yokoi, Masahiro Fukuda, Tomohiro J. Narita, Hiroki Arai, Mai Tambo, Takashi Sumikama, Manae Tatsumi, Keitaro Yamashita, Junki Koyanagi, Mai Kugawa, Hisako Ikeda, Ayumi Sumino, Ayori Mitsutake, Brian K. Kobilka, Asuka Inoue, Hideaki E. Kato,*
- 掲載誌
- Nature
- 掲載日
- 2026.03.12
- DOI
- 10.1038/s41586-026-10228-w
- URL
- https://www.nature.com/articles/s41586-026-10228-w

