リガンド依存的Wntシグナルによる胃がん転移機構を解明
金沢大学ナノ生命科学研究所(WPI-NanoLSI)/がん進展制御研究所の大島正伸教授、大島浩子准教授と、医薬保健研究域医学系消化管外科学の稲木紀幸教授、同大学院医薬保健学総合研究科博士課程4年の古谷裕一郎らの共同研究グループは、マウスおよびオルガノイドモデルを用いて、リガンド依存的Wntシグナル(※1)が胃がんの肝転移巣形成を促進する分子機構を、明らかにしました。
転移をともなう胃がん患者の5年生存率は約5%と低く、新規治療薬開発のためにも、胃がん転移機構の解明は重要な研究課題です。胃がんでは、消化器がん発生に重要なWntシグナルを直接活性化する遺伝子変異の頻度が他のがんに比べて低く、外因性のWntリガンドによる「リガンド依存的Wntシグナル活性化」が重要と考えられています。しかし、Wntリガンドがどの細胞に作用して、どのように転移巣形成に関与するのかについて、十分に理解されていませんでした。
本研究では、胃がんに関わる遺伝子変異を導入したマウスモデルを作製し、そこから樹立したオルガノイドを用いた解析により、胃がん細胞が産生するWntリガンドが、肝転移巣におけるがん関連線維芽細胞(CAF)のWntシグナルを活性化し、WntとTGFβの相乗作用によってHas2発現が誘導され、微小環境へのヒアルロン酸沈着を高めることで、がん細胞の生存・増殖を支えて転移巣形成に作用することを示しました。
これらの知見は将来、胃がん転移に対する予防・治療薬開発研究に活用されることが期待されます。
本研究成果は、2026年2月14日(英国時間)に英国科学誌『Nature Communications』のオンライン版にunedited versionとして掲載されました。
【研究の背景】
Wntシグナルは幹細胞性の維持に重要であり、大腸がんではAPCやCTNNB1などの遺伝子変異によるWntシグナル活性化が発がんを誘導することがよく知られています。一方で胃がんでは、Wntシグナルを直接活性化する遺伝子変異の頻度は低く、外因性Wntリガンド刺激によるリガンド依存的Wntシグナル活性化が発がんに関与することが報告されています。しかし、リガンド依存的Wntシグナルが、胃がん転移などの悪性化にどう関与するかは、これまで十分に明らかにされていませんでした。
また、胃がんは東アジアにおいて罹患率の高いがんであり、転移を伴うステージIVの胃がん患者の予後は依然として厳しいことから、転移形成の分子基盤を理解し、新たな予防・治療標的を提示することが重要です。
【研究手法(モデル)】
本研究では、胃がんで高頻度に変異が認められるKras、Tgfbr2、Trp53の3遺伝子変異を胃粘膜上皮に導入したマウスモデル(KTP)と、これに加えてWntリガンドWnt1を発現するマウスモデル(WKTP)を作製し、解析を行いました(図1)。さらに、双方のマウス胃粘膜からオルガノイド(※2)を樹立し、脾臓移植による肝転移モデルで転移巣形成を解析しました。
【研究成果の概要】
- オルガノイドの増殖様式
KTPおよびWKTPオルガノイドはいずれも、基本的には外因性Wntリガンド刺激が生存・増殖に必要です。一方で、WKTPオルガノイドは、自身が産生するWnt1によるオートクリン刺激により、生存できることが明らかになりました。
- 肝転移巣形成能の違い
KTPおよびWKTPオルガノイドをそれぞれマウス脾臓に移植したところ、WKTPオルガノイドにおいてのみ肝転移巣の形成が観察されました(図2)。この結果は、リガンド依存的Wntシグナルが胃がんの肝転移巣形成に重要であることを示します。
- 「がん細胞内Wnt活性化」だけでは転移は成立しない
胃がん細胞内のWntシグナル活性化が肝転移形成に必要十分かを検証するため、KTP細胞でApc遺伝子を欠損させ、リガンド非依存的にWntシグナルを活性化したApc-KTP細胞を作製しました。しかし、Apc-KTPは高いWnt活性を獲得したにもかかわらず肝転移巣を形成しませんでした。この結果は「がん細胞内のWntシグナル活性化」だけでは転移巣形成には不十分であり、「がん細胞由来のWntリガンドが、転移先の間質細胞に作用する」可能性が考えられました(図3)。
- 転移微小環境でのCAF活性化とHas2誘導
空間トランスクリプトーム解析(※3)により、WKTP肝転移巣のCAF(※4)集団ではWntシグナルが活性化しており、同時にTGFβシグナルも活性化していることが確認されました。さらに、CAFではWntシグナルとTGFβシグナルの相乗作用により、Has2(※5)遺伝子発現が高く誘導され、ヒアルロン酸(※6)合成が誘導されていることが分かりました。
この所見は、マウスおよびヒトの胃がん肝転移巣においてヒアルロン酸の沈着が高頻度に観察されることとも整合的でした。
- ヒアルロン酸分解による肝転移形成の抑制
WKTP細胞にヒアルロニダーゼ(Hyal1/2)を発現させ、がん細胞周囲のヒアルロン酸を分解できるようにしたところ、脾臓移植による肝転移巣形成が顕著に抑制されました(図4)。この結果は、Has2‐ヒアルロン酸沈着が胃がんの肝転移巣形成の鍵であることを示します。
以上の結果により、胃がん細胞が産生するWntリガンドは、がん細胞自身のWntシグナル活性化に加えて、転移先である肝臓のCAFにおけるWntシグナルを活性化し、さらにWntとTGFβの協調作用によるHas2誘導とヒアルロン酸沈着を介して、がん細胞の生存・増殖を支え、肝転移巣形成を促進することが示されました(図5)。したがって、リガンド依存的WntシグナルおよびHas2-ヒアルロン酸経路は、胃がん肝転移に対する新たな予防・治療標的として重要であると考えられます。
【今後の展開】
がん間質におけるヒアルロン酸沈着は、大腸がん原発巣で悪性化との関連が報告されていますが、転移巣形成を支える具体的な分子機構については、未解明な点が残されています。ヒアルロン酸は、CD44を介したシグナルのリガンドとして幹細胞性の維持に関与することが知られており、転移巣においてもがん細胞の性質維持に寄与する可能性があります。また、ヒアルロン酸は物理的バリアとして免疫細胞の浸潤・攻撃を妨げる可能性や、保水性の高い層を形成して生存因子・増殖因子が保持されやすい微小環境を作る可能性も考えられます。
今後は、ヒアルロン酸が転移巣形成を支える下流機構の解明を進めるとともに、Has2‐ヒアルロン酸経路を標的とした予防・治療法の開発につなげていきます。
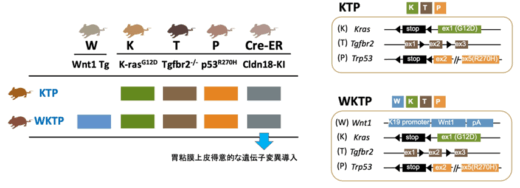
図1. KTPおよびWKTPマウスの胃粘膜に導入した遺伝子変異。どちらもKras、Tgfbr2、Trp53変異を有し、WKTPマウスではそれに加えてWnt1を発現する。
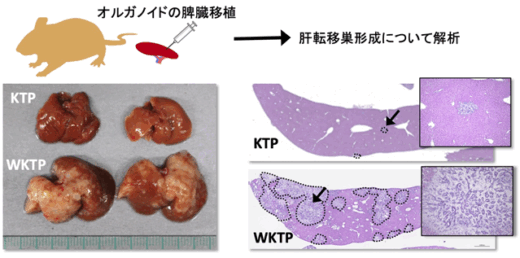
図2.KTP、WKTPオルガノイドを脾臓移植すると、WKTPのみ肝転移巣を形成した。
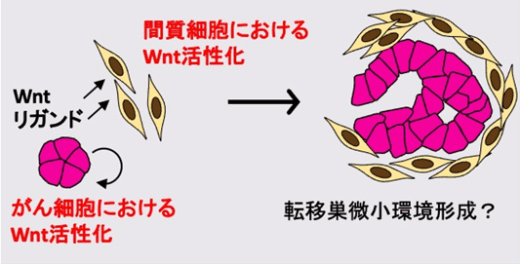
図3. がん細胞のWnt活性化だけでは転移巣を形成しないので、間質細胞のWnt活性化の関与が考えられた。
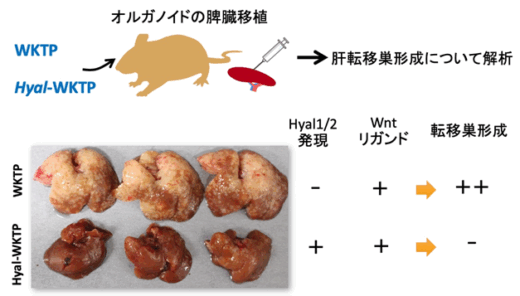
図4. ヒアルロニダーゼ(Hyal1/Hyal2)を発現するHyal-WKTPオルガノイドは、Wntリガンドを発現していても肝転移巣を形成しない。
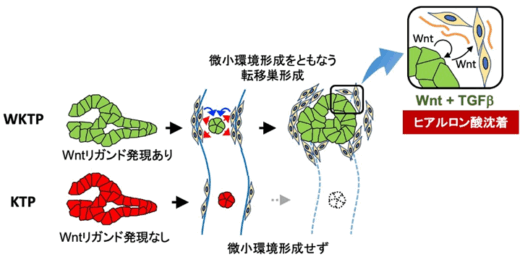
図5. リガンド依存的Wntシグナルによる胃がん肝転移機構。
用語解説
掲載論文情報
- 論文タイトル
- Ligand-dependent Wnt signaling promotes gastric cancer metastasis through hyaluronan expression in microenvironment (リガンド依存的Wntシグナルによるヒアルロン酸微小環境を介した胃がん転移機構)
- 著者
- Yuichiro Furutani, Hiroko Oshima, Chang Pyo Hong, SeonJu Choi, Ryosuke Machi, Mizuho Nakayama, Kazuhiro Murakami, Shintaro Yagi, Yukinobu Ito, Daichi Maeda, Noriyuki Inaki, Nick Barker, and Masanobu Oshima (古谷裕一郎、大島浩子、Chang Pyo Hong、SeonJu Choe、真智涼介、中山瑞穂、村上和弘、八木真太郎、伊藤行信、前田大地、稲木紀幸、Nick Barker、大島正伸)
- 掲載誌
- Nature Communications
- 掲載日
- 2026.02.14
- DOI
- 10.1038/s41467-026-69470-5
- URL
- https://www.nature.com/articles/s41467-026-69470-5

