生体にやさしいナノ粒子で光熱刺激: 神経・筋細胞のリモート制御に成功
金沢大学ナノ生命科学研究所(WPI-NanoLSI)の新井敏教授、山崎健特任助教、理工研究域生命理工学系の木矢剛智准教授、理工研究域生命理工学系/ナノ生命科学研究所(WPI-NanoLSI)の木矢星歌助教、イタリア技術研究所のジャンニ・チオファーニ主任研究員、アレッシオ・カルミニャーニ博士研究員らの国際共同研究グループは、生体毒性の低い有機ナノ粒子が持つ光熱効果を用いて、神経細胞や筋細胞の機能をリモートかつ非侵襲的に制御することに成功しました。
神経や筋組織の活動を遠隔で制御する技術は、将来的な神経・筋疾患の新たな治療戦略として大きな期待が寄せられています。中でも、光を用いた制御は、刺激の場所とタイミングを精密に操作できるという点で優れており、近赤外(NIR)光(※1)と光熱変換ナノ材料の組み合わせにより生体深部の標的組織への選択的な刺激が可能となります。従来は、近赤外光を効率よく吸収し、高い効率で熱を発生させる金ナノ材料などが広く利用されてきましたが、活性酸素種の生成や長期的な生体適合性に課題がありました。
本研究では、高い生体適合性、抗酸化作用、および光熱変換能を兼ね備えたポリドーパミンナノ粒子(Polydopamine Nanoparticles: PDNPs)を用いて、近赤外レーザー光により、神経様細胞や筋管(筋分化細胞)の機能を単一細胞レベルで制御することに成功しました。さらに、PDNPsは温度上昇に伴う酸化ストレスを抑制する効果を持つことも明らかとなり、神経の可塑性や筋成長の促進に関与するタンパク質の発現変化も確認されました。加えて、ショウジョウバエ脳を用いた実験でも神経活動の光制御に成功しました。
これらの知見は、光応答性の有機ポリマーナノ粒子を活用した細胞機能制御技術を基軸として、将来的な神経・筋疾患の非侵襲的な治療法の開発に繋がることが期待されます。
本研究成果は、2025年4月24日(米国東部時間)に米国科学誌『ACS Nano』のオンライン版に掲載されました。また、本成果は、大阪・関西万博のイタリアパビリオンにて行われたWorkshop-Istituto Italiano Di Tecnologia (IIT)(2025年6月25日)にて、チオファーニ主任研究員と新井敏教授が口頭発表しました。
【研究の背景】
神経や筋組織の活動を遠隔で刺激・操作する技術は、神経・筋疾患の治療応用に向けて長年注目されてきました。中でも磁場や光を用いた非侵襲的手法は、外科的侵襲を避けることで炎症などの副次的な生体応答を抑制できる利点があります。一方で、磁気刺激など一部の手法は空間分解能が比較的低く、標的部位周辺の組織にも非選択的に作用する可能性がある点が課題とされていました。この課題は、ナノトランデューサー(※2)の発展により解決されつつあります。特に NIR光を吸収するナノ材料は、生体深部への非侵襲的な刺激が可能なため注目されています。その中でも、金ナノ材料は優れたNIR吸収と光熱変換能を有し、温度感受性を持つ神経や筋組織への刺激に関する研究が進んでいます。しかし、活性酸素種の生成や生体適合性の低さといった課題も指摘されていました。
【研究成果の概要】
金ナノ材料に代わる生体毒性の低いNIR光熱変換ナノトランデューサーを開発するために、我々は高分子材料の一つであるポリドーパミン(Polydopamine) に着目しました。ポリドーパミンは、高い生体適合性、生分解性、抗酸化特性、および優れた光熱変換能を有しており、バイオマテリアルとしてさまざまな応用例が報告されています。本研究では、ポリドーパミンからナノ粒子(polydopamine nanoparticles: PDNPs)を調製し(図1a,b,c)、PDNPsが光熱効果により、細胞を熱刺激できるのかを検討しました。温度応答蛍光プローブを用いたタイムラプスイメージングから、PDNPsは繰り返しの光照射に応答して、細胞内の温度を上昇させることが分かりました(図1d,e,f)。
次に、神経様細胞や筋管を熱刺激することで、それぞれの機能が遠隔操作できるか試験しました。その結果、神経様細胞では、興奮性神経伝達物質の一つであるアセチルコリンの分泌(図2a,b)、筋管では、可逆的な細胞の変形が観察されました(図2c,d)。これらの結果は我々の狙い通り、光照射されたPDNPsが光熱変換により細胞を熱刺激し、それぞれ生体サンプルがもつ機能を誘導したことを示しています。
最後に、ショウジョウバエ脳のex vivo サンプルに対する本手法の応用可能性について検討を行いました。脳を構成する各細胞に、あらかじめカルシウムバイオセンサーを発現させ、PDNPsによる熱刺激に応答してカルシウムセンサーの蛍光輝度が上昇するように実験系を設計しました(図3a)。光照射のタイミングに一致して、センサーの蛍光輝度が、即時に上昇することが観察されました(図3b,c)。さらに、アセチルコリン分解酵素またはアセチルコリン受容体の阻害剤で処理した脳に対し、PDNPsを用いた熱刺激を行ったところ、カルシウムセンサーの発光パターンに顕著な変化が見られました(掲載論文参照)。このことから、熱刺激を受けた神経細胞がアセチルコリンを分泌し、それを受容した周囲の神経細胞が興奮するという機構が示唆されました。
【今後の展開】
本研究により、ポリドーパミンを基材とするナノ粒子(PDNPs)が、従来の金ナノ材料に代わる、生体毒性の低いNIR光応答性光熱変換ナノトランスデューサーとして有用であることが示されました。さらに、ポリドーパミンはその多様な官能基構造により、薬剤の担持や表面修飾が可能であることから、PDNPsに新たな機能を付与することで、多様な応用展開が期待されます。
本研究は、イタリア技術研究所のフラッグシップ・プログラム「健康的な生活のための技術」の一部として実施されました。
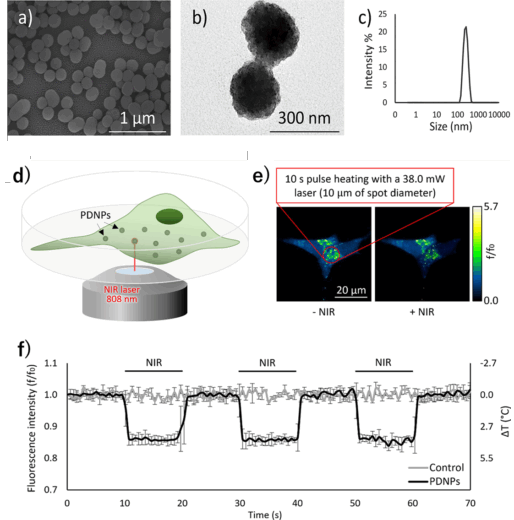
図1 PDNPsの粒子特性と光熱効果 a)ナノ粒子のSEM(※3)画像 b)ナノ粒子のTEM(※4)画像 c)ナノ粒子の粒径分布 d)CLSM(※5)観察下での細胞内におけるPDNPsの光熱効果評価 e)d)の実際の蛍光画像 f)e)の解析 (掲載論文のFig.1と2を改変 著作権は著者に帰属(© 2025) アメリカ化学会により出版)
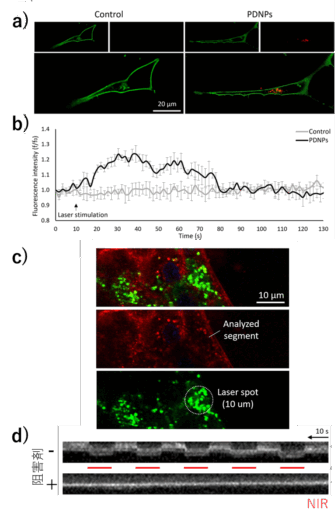
図2 PDNPsの光熱効果による細胞機能の誘導 a)神経様細胞のアセチルコリン分泌の誘導 左 : PDNPsなし。右 : PDNPsあり。b)a)の解析 c)筋収縮の誘導 d)c)の解析 (掲載論文のFig.5と6を改変 著作権は著者に帰属(© 2025) アメリカ化学会により出版)
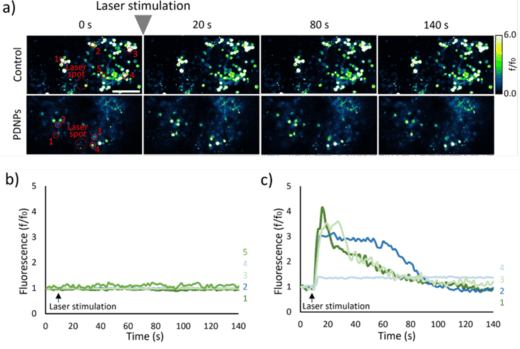
図3 ex vivoショウジョウバエ脳におけるPDNPsの有効性の検討 a)カルシウムイメージングによる神経発火の観察 b)PDNPsなしで光照射した時のカルシウムセンサー輝度変化 c)PDNPsありで光照射した時のカルシウムセンサー輝度変化 (掲載論文のFig.8を改変 著作権は著者に帰属(© 2025) アメリカ化学会により出版)
用語解説
掲載論文情報
- 論文タイトル
- Cellular activity modulation mediated by NIR-irradiated polydopamine nanoparticles: In vitro and ex vivo investigation (近赤外線照射されたポリドーパミンナノ粒子による細胞活性調節: In vitroおよびex vivoでの検討)
- 著者
- Alessio Carmignani, Takeru Yamazaki, Matteo Battaglini, Cong Quang Vu, Attilio Marino, Seika Takayanagi-Kiya, Taketoshi Kiya, Satoshi Arai, Gianni Ciofani (アレッシオ・カルミニャーニ、山崎健、マッテオ・バッタリーニ、コン・クアン・ブー、アッティリオ・マリーノ、木矢星歌、木矢剛智、新井敏、ジャンニ・チオファーニ)
- 掲載誌
- ACS Nano
- 掲載日
- 2025.04.24
- DOI
- 10.1021/acsnano.5c04181
- URL
- https://pubs.acs.org/doi/10.1021/acsnano.5c04181

