がん撃退の新戦略:キラーT細胞を活性化する改変エクソソームの開発に成功
金沢大学ナノ生命科学研究所(WPI-NanoLSI)の呂夏氷特任助教、WPI-NanoLSI/医薬保健研究域医学系の山野友義准教授、華山力成教授の研究グループは、細胞が分泌する微粒子であるエクソソームを人工的に改変し、がん特異的キラーT細胞(※1)を選択的に活性化する「改変エクソソーム」を開発しました。この技術により、生体内でがんに対する免疫応答を大幅に促進することに成功しました。
エクソソームは、直径約100ナノメートルの膜小胞で、タンパク質や核酸を運搬し、細胞間の情報伝達を担う「メッセージボックス」として機能します。研究グループは、エクソソームを産生する細胞を遺伝子改変し、エクソソーム上にキラーT細胞を活性化するための3つの分子(抗原刺激、補助シグナル分子、サイトカイン(IL-2))を同時に搭載した「抗原提示小胞(AP-EV)」を作製しました。
培養実験およびマウスを用いた実験において、AP-EVはがん細胞を特異的に殺傷するキラーT細胞を選択的に活性化し、がんに対する免疫応答を著しく増強することが確認されました(図1)。
さらに、ヒトのT細胞を活性化する「ヒト化AP-EV」も開発し、ヒトのがん抗原に応答するキラーT細胞を効果的に増殖させることに成功しました。これらの成果は、新たながん免疫療法の実現に向けた重要な一歩と期待されます。
本研究成果は,2025年3月28日(米国東部時間)に国際学術誌『Journal of Extracellular Vesicles』に掲載されました。
【研究の背景】
エクソソームは、細胞が体内で情報をやり取りするために使う小さな「メッセージボックス」のようなものです。これらは細胞の中で作られ、細胞の外に放出される直径50~150ナノメートル程度の非常に小さな小胞です。エクソソームの中には、細胞が作ったタンパク質や脂質、核酸などが詰まっています。これらの分子が、他の細胞に送られることで、細胞同士が情報を交換できます。エクソソームは現在の医学やバイオテクノロジーの分野で非常に注目されており、病気の治療や新しい医薬品の開発に大きな可能性を秘めています。
【研究成果の概要】
エクソソームは、免疫細胞においても「情報を伝達するツール」として機能します。エクソソームの中にはタンパク質やRNAなどの分子が含まれており、これらが他の免疫細胞に働きかけることで、免疫反応を活性化したり抑制したりすることができます。本研究では、エクソソームを人工的に改変し、がん細胞を攻撃するキラーT細胞を選択的に増強する「改変エクソソーム」を開発しました。
キラーT細胞の増強には、T細胞受容体(TCR)を介した抗原刺激、補助シグナル分子の活性化、およびIL-2というT細胞の増殖を促進するサイトカインが重要です。この要素をエクソソームに組み込むため、テトラスパニンという4回膜貫通タンパク質を足場として利用し、それらの分子を融合させた改変エクソソームを作製しました。このエクソソームは、抗原を提示する能力を持つことから、「抗原提示小胞(Antigen-Presenting Extracellular Vesicles、AP-EV)」と名付けられました(図2)。
AP-EVは約100ナノメートルの大きさで、キラーT細胞より100倍小さい小胞ですが、培養実験において、キラーT細胞を選択的に増やすことができることが確認されました。また、マウスを用いた実験では、AP-EVがキラーT細胞を効果的に増強し、がん細胞を移入したマウスの生存期間を顕著に延長することが分かりました(図3)。さらに、ヒトの免疫系における効果を評価するために、ヒト末梢血から単離したT細胞にNY-ESO-1というがん抗原特異的TCRを導入し、ヒト化AP-EVを用いて活性化しました(図4)。その結果、ヒト化AP-EVもキラーT細胞を効果的に増強することが確認されました。
これらの成果は、がんに対する免疫応答を強化する新たなアプローチとして、がん免疫療法の発展に大きく寄与する可能性があります。
【今後の展開】
本研究により、改変エクソソームを用いてキラーT細胞を選択的に増強し、がんに対する免疫応答を高めることに成功しました。今後は、AP-EV(抗原提示小胞)の安全性や有効性を評価するため、ヒトを対象とした非臨床試験や臨床試験を進める予定です。これにより、AP-EVを用いた新しいがん免疫療法の実現を目指します。
改変エクソソームの大きな特徴は、その設計を変えることで、特定の免疫細胞を選択的に活性化したり抑制したりできる点です。今回の研究では、キラーT細胞を増強するエクソソームを設計しましたが、ヘルパーT細胞(※2)を活性化させる改変エクソソームを作製することも可能です。また、免疫の異常な活性化が原因で発症する自己免疫疾患やアレルギーに対して、過剰に活性化した免疫細胞を選択的に抑える改変エクソソームの開発も期待されています。本技術は、がん治療のみならず、さまざまな免疫疾患への応用が見込まれます。
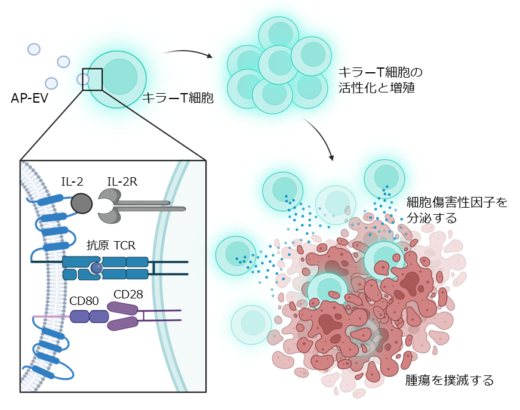
図1:AP-EVはキラーT細胞を増強し、がんに対する免疫応答を促進する。
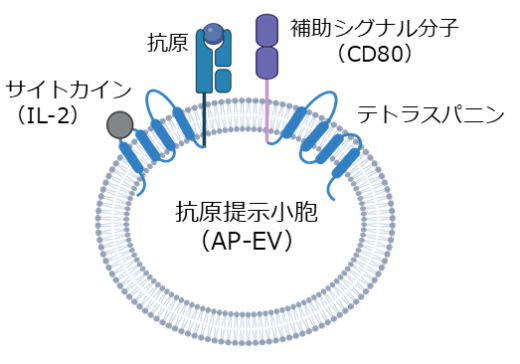
図2:抗原提示小胞(AP-EV)は抗原、補助シグナル分子、サイトカイン(IL-2)を同時に発現する。
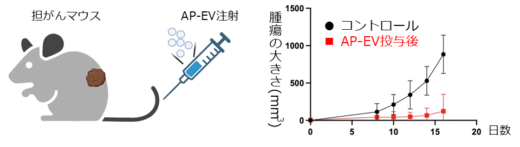
図3:AP-EVはキラーT細胞を増強し、がん細胞を移入したマウスの生存期間を顕著に延長する。
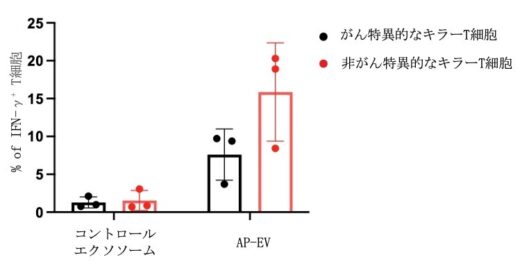
図4:ヒト化AP-EVを用いて、選択的にがん特異的キラーT細胞を増強した。
用語解説
掲載論文情報
- 論文タイトル
- Direct delivery of immune modulators to tumour-infiltrating lymphocytes using engineered extracellular vesicles (改変細胞外小胞を用いた腫瘍浸潤リンパ球への免疫調節剤の直接送達)
- 著者
- Xiabing Lyu#, Tomoyoshi Yamano#†, Kanto Nagamori, Shota Imai, Toan Van Le, Dilireba Bolidong, Makie Ueda, Shota Warashina, Hidefumi Mukai, Seigo Hayashi, Kazutaka Matoba, Taito Nishino and Rikinari Hanayama† (呂夏氷#、山野友義#†、永森幹人、今井翔太、Toan Van Le、Dilireba Bolidong、上田真喜栄、藁科翔太、向井英史、林清吾、的場一隆、西野泰斗、華山力成†) #:筆頭著者 †:責任著者
- 掲載誌
- Journal of Extracellular Vesicles
- 掲載日
- 2025.03.28
- DOI
- 10.1002/jev2.70035
- URL
- https://isevjournals.onlinelibrary.wiley.com/doi/full/10.1002/jev2.70035

