ナノスケールの細胞外小胞を高速原子間力顕微鏡で可視化 ナノ動態観察と免疫表現型分類に成功!
金沢大学大学院新学術創成研究科ナノ生命科学専攻/「知」の共創と往還で実現する新価値創造人材育成プロジェクト選抜学生のムハンマド・イスマン・サンデイラ(博士後期課程3年、研究当時)、ナノ生命科学研究所のキイシヤン・リン特任助教、安藤敏夫特任教授、華山力成教授、リチャード・ウォング教授らの共同研究グループは、高速原子間力顕微鏡(高速AFM)(※1)を用い、細胞外小胞(※2)マーカーの動態をナノスケールで観察することに初めて成功しました。
小型細胞外小胞(small extracellular vesicles、sEVs)は、親細胞由来の脂質、タンパク質、RNAを運搬し、特定の細胞タイプや生物学的状態を示すバイオマーカーとして機能します。エクソソームやマイクロベシクルを含むsEVsは、細胞間の成分輸送を通じた情報伝達に重要な役割を果たします。現在、超遠心分離法やTim-4アフィニティ法などの手法により高純度のsEVsを分離することが可能ですが、そのサイズの小ささにもかかわらず、sEVsは細胞内起源の多様性により依然として不均一な性質を持っています。
本研究では、高速原子間力顕微鏡(高速AFM)を用い、エクソソームマーカー(IgG CD63およびIgG CD81)と組み合わせることで、単一sEVレベルでの細胞内起源の解析を実施しました。まず、生理的条件下でのHEK293T細胞由来sEVsのナノトポロジーを初めて明らかにしました。その結果、直径100 nmを超える大型sEVsは、100 nm以下の小型sEVsと比較して高さの変動が大きいことが確認されました。さらに、マウス由来のIgG CD63およびウサギ由来のIgG CD81とIgGコントロールが、特徴的な「Y字型」の構造を持ち、同様の構造動態特性を示すことを発見しました。最後に、エクソソームマーカー抗体が主に直径100 nm以下のsEVsと共局在し、100 nm超のsEVsではほとんど見られなかったことから、CD63-CD81が豊富なsEV(エクソソーム様)と、CD63-CD81が少ないsEV(エクトソーム様)の2種類のサブタイプが存在することが明らかになりました。
本研究は、高速AFMを用いたナノスケール解析により、異なるsEVサブタイプの特徴付けが可能であることを実証しました。この技術は、sEVの多様な集団を識別する新たな手法として、疾患バイオマーカーの研究や診断技術の発展に貢献することが期待されます。
本研究成果は、2025 年 3 月 26日(米国東部時間)に国際細胞外小胞学会誌『Journal of Extracellular Vesicles』のオンライン版に掲載されました。
研究の背景
細胞が分泌する小型細胞外小胞(small extracellular vesicles、sEVs)は、細胞間情報伝達や疾患のバイオマーカーとして注目されています。sEVsにはエクソソームやマイクロベシクルが含まれ、細胞由来の脂質・タンパク質・RNAを運搬することで、生理的・病理的プロセスに関与しています。近年、超遠心分離法やTim-4アフィニティ法により、高純度のsEVsの分離が可能になりました。しかし、sEVsの細胞内起源は多様であり、単一sEVレベルでの詳細な解析は困難でした。本研究では、高速原子間力顕微鏡(高速AFM)を活用し、sEVsのナノスケール解析を行うことで、エクソソームマーカーの動態を可視化し、sEVのサブタイプを特定することを目指しました。
研究成果の概要
本研究では、HEK293T細胞由来のsEVsを対象に、高速AFMを用いたナノスケール解析を実施しました。その結果、sEVsのナノトポロジーを詳細に観察し、生理的条件下におけるsEVsの構造的特徴を可視化することに成功しました。特に、直径100 nm超のsEVsは、100 nm以下のsEVsと比較して高さの変動が大きいことが明らかになり、サイズによる構造的な違いが示されました。さらに、エクソソームマーカーであるCD63およびCD81の動態を解析したところ、マウス由来のIgG CD63およびウサギ由来のIgG CD81が、ナノスケールレベルで特徴的な「Y字型」構造を持つことを確認しました。この結果から、これらのマーカーがsEVの分類において重要な指標となることが示唆されました(図1)。
今後の展開
本研究により、高速AFMを活用したsEVsのナノスケール解析の有用性が実証されました。今後は、sEVの細胞内起源のさらなる解明を目指し、高速AFMによるナノスケール免疫表現型解析を発展させることで、細胞内でのsEVの形成メカニズムをより詳細に明らかにしていきます。また、疾患バイオマーカーとしての応用にも取り組み、sEVの表面マーカーを活用した新たな疾患診断技術の開発を進め、がんや神経疾患の早期診断ツールとしての実用化を目指します。さらに、高速AFMとフローサイトメトリーやナノフローメトリーなどの既存手法を統合し、高精度なsEV解析技術の確立を図ることで、より包括的な解析が可能なプラットフォームの構築を進めていきます。本研究は、sEVを標的とした診断技術やバイオマーカー研究の新たな可能性を切り開くものであり、今後の発展が期待されます。
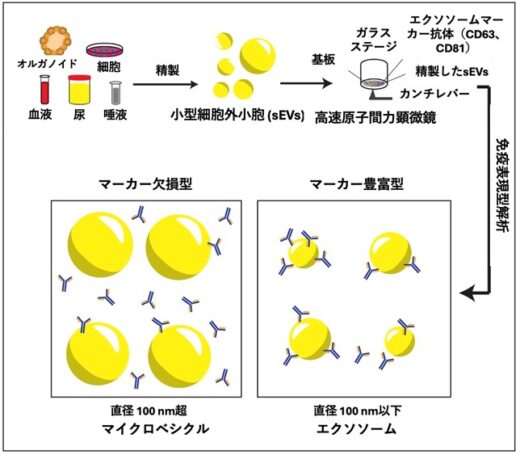
図1:小型細胞外小胞(sEVs)の免疫表現型解析(Immunophenotyping) この図は、小型細胞外小胞(sEVs)を高速原子間力顕微鏡(高速AFM)で解析し、エクソソームマーカー(CD63、CD81)を用いて免疫表現型分類を行う流れを示しています。
用語解説
掲載論文情報
- 論文タイトル
- Nanoscopic Profiling of Small Extracellular Vesicles via High-Speed Atomic Force Microscopy (HS-AFM) Videography (高速原子間力顕微鏡(高速AFM)ビデオグラフィーによる小型細胞外小胞のナノスケールプロファイリング)
- 著者
- Muhammad Isman Sandira, Keesiang Lim, Takeshi Yoshida, Elma Sakinatus Sajidah, Shinnosuke Narimatsu, Reon Imakawa, Kota Yoshimura, Goro Nishide, Yujia Qiu, Azuma Taoka, Masaharu Hazawa, Toshio Ando, Rikinari Hanayama, Richard W Wong (ムハンマド・イスマン・サンデイラ、キイシヤン・リン、吉田孟史、エルマ・サキナトゥス・サジダ、成松慎之佑、今川怜音、吉村光太、西出梧朗、邱宇嘉、田岡 東、羽澤勝治、安藤敏夫、華山力成、リチャード・ウォング)
- 掲載誌
- Journal of Extracellular Vesicles
- 掲載日
- 2025.03.26
- DOI
- 10.1002/jev2.70050
- URL
- https://isevjournals.onlinelibrary.wiley.com/doi/full/10.1002/jev2.70050

